Тиофеновое кольцо
Cтраница 2
Возможно гидрирование водородом тиофенового кольца в тиофановое и на твердых катализаторах. [16]
Замещение атомов водорода тиофенового кольца на алкилра-д и калы смещает спектр поглощения в длинноволновую область, и в зависимости от положения заместителя меняется экстинкция. В среднем у моноалкилтиофенов. [17]
Замещение атомов водорода тиофенового кольца на алкилы смещает спектр поглощения в длинноволновую область, и в зависимости от положения ал кил ь-иого заместителя меняется интенсивность поглощения: замещение в положение 2 - увеличивает, а в положение 3 - уменьшает экстинкцию. [18]
Интересно было изучить поведение тиофенового кольца в вышеназванной реакции. [19]
В основе строения биотина лежит тиофеновое кольцо, к которому присоединена мочевина, а боковая цепь представлена валерьяновой кислотой. [20]
Производные тиофена, в которых тиофеновое кольцо сопряжено с бензольными или нафталиновыми кольцами, также аналогичны по свойствам гомологам нафталина. Близость в свойствах ароматических и циклических сернистых соединений обусловливает трудность их отделения друг от друга. [21]
Он высказывает предположение, что тиофеновое кольцо может быть соединено с бензольным с помощью алифатического мостика. [22]
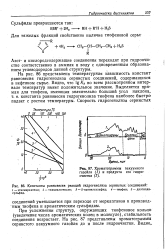 |
Хроматограммы вакуумного газойля ( 1 и продукта его гидроочистки ( 2.| Константы равновесия реакций гидрогенолиза сернистых, соединений. [23] |
При усложнении структур, окружающих тиофеновое кольцо ( увеличение числа ароматических колец в молекуле), стабильность соединения возрастает. На рис. 87 представлены хроматограммы сернистого вакуумного газойля до и после гидроочистки. [24]
Из двух конденсированных в орто-положении тиофеновых колец состоит молекула тиофтена. [25]
Сера, непосредственно связанная с тиофеновым кольцом, увеличивает способность молекулы к взаимодействию с неподвижной фазой. Однако этот эффект не зависит от сопряжения серы с циклом. Основную роль во взаимодействии с фазой играет тиофеновое кольцо с его подвижной системой я-электронов; экранизация кольца уменьшает взаимодействие, сульфидная сера не только не участвует в сопряжении с тиофеновым кольцом, но и не является проводником сопряжения. [26]
Тиофенкарбоновая кислота без заместителей в тиофеновом кольце гидрируется с наибольшей легкостью. Введение в кольцо метальной группы затрудняет гидрогенолиз; выход продукта гидрогенолиза несколько снижается, с 70 до 67 %, если метальная группа находится в ( / - положении и до 59 % - в р - поло-жении. Меркаптаны менее прочны, чем сульфид. [27]
Тиофенкарбоновая кислота без заместителей в тиофеновом кольце гидрируется, как видно из приведенных данных, наиболее легко. Введение в кольцо метилыюй группы затрудняет гидрогенолиз; выход продукта гидрогеполиза несколько снижается ( с 70 до 67 %), если метальная группа находится в а - ноложении и значительно снижается ( до 59 %), если метиль-ная группа находится в / З - положеиии. Меркаптаны менее прочны, чем сульфиды. [28]
Тиофенкарбоновая кислота без заместителей в тиофеновом кольце гидрируется, как видно из приведенных данных, наиболее легко. Введение в кольцо метальной группы затрудняет гидрогенолиз; выход продукта гидрогенолиза несколько снижается ( с 70 до G7 / 6), если метильная группа находится в а - положении, и значительно снижается ( до 59 %), если метильная группа находится в ( 3 -положении. Меркаптаны менее прочны, чем сульфиды. [29]
Тиофенкарбоновая кислота без заместителей в тиофеновом кольце гидрируется, как видно из приведенных данных, наиболее легко. Введение в кольцо метильной группы затрудняет гидрогенолиз; выход продукта гидрогенолиза несколько снижается ( с 70 до 67 %), если метильная группа находится в а - положении, и значительно снижается ( до 59 %), если метильная группа находится в р - положении. Меркаптаны менее прочны, чем сульфиды. [30]
Страницы: 1 2 3 4