Комплекс - ниобий
Cтраница 1
Комплекс ниобия с бромпирогаллоловым красным не растворяется в воде. Для стабилизации его коллоидного раствора прибавляют немного желатины. [1]
Бензоилфенилгидроксиламиновый комплекс ниобия довольно устойчив и прочно удерживается на поверхности угля, в то время как примесь Sb125 при указанном значении рН проходит в фильтрат. [2]
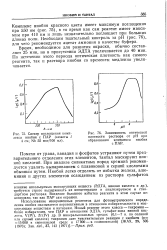 |
Спектр поглощения комплекса ниобия с ПАР ( кюветы / 4 Nb 55 мкг / 100 мл.| Зависимость оптической. [3] |
Комплекс ниобия красного цвета имеет максимум поглощения при 550 нм ( рис. 75), в то время как сам реагент имеет максимум при 410 нм и лишь незначительно поглощает при больших длинах волн. Необходим тщательный контроль за рН ( рис. 76), для чего рекомендуется ацетат аммония в качестве буфера. [4]
Хотя щавелевокислые комплексы ниобия и тантала были открыты около шестидесяти лет тому назад [1] и их значение в промышленной переработке руд этих металлов, а также при их аналитическом разделении известно, исследованию этих комплексов уделяется чрезвычайно мало внимания. Лишь спустя тридцать лет после открытия оксалатных комплексов ниобия и тантала появляется работа [2], в которой авторы на основании проведенных кондуктометрических и потенциометрических исследований подтверждают факт образования комплексных соединений ниобия и тантала со щавелевой кислотой. В то же время они высказывают предположение, что растворение пятиокисей ниобия и тантала в щавелевой кислоте имеет коллоидный характер. Этими работами в основном и исчерпывается литература, посвященная изучению оксалатных растворов ниобия и тантала. [5]
Образование комплекса ниобия с ЭДТА впервые зафиксировали Феррет и Мильнер [ 56 ( 123) ] в результате полярографических исследований. [6]
Структуры комплексов ниобия [46, 285, 286, 299, 300, 302, 303] и ванадия [ 323а ] подтверждены рентгеноструктурным анализом. [7]
В комплексах ниобия с HFn интенсивность полосы - 875 смг1 сильно возрастает при уменьшении кислотности раствора, из которого выделялся комплекс. Комплекс, полученный из концентрированной соляной кислоты, имеет молярное соотношение Nb: Fn: Cl, равное 1: 2: 1, и содержит полимерные формы, о чем свидетельствует полоса 857 см-1 средней интенсивности. Комплексы, полученные из 8 - 1 N раствора НС1, имеют одинаковый состав с соотношением компонентов 1: 1: 1 и широкую интенсивную полосу 834 - 880 см - полимерных форм. [8]
При Х385 ммк комплекс ниобия с реактивом имеет максимальное светопоглощение, а комплекс титана мало поглощает свет; однако введение поправки на титан все же необходимо. Если присутствует железо ( III), даже в следах, прибавляют соль олова ( II) для его восстановления. [9]
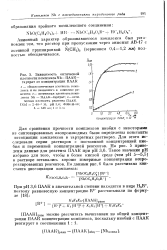 |
Зависимость оптической. [10] |
Для сравнения прочности комплексов ниобия с некоторыми из синтезированных азопроизводных были определены константы иссоциации комплексов в тартратных растворах. [11]
При Я 385 ммк комплекс ниобия с реактивом имеет максимальное светопоглощение, а комплекс титана мало поглощает свет; однако введение поправки на титан все же необходимо. Если присутствует железо ( III), даже в следах, прибавляют соль олова ( II) для его восстановления. [12]
Комплексы тантала легче, чем комплексы ниобия, экстрагируются органическими растворителями типа диизопропилкетона. [13]
Метод основан на измерении светопоглощения комплекса ниобия с кислотным хром фиолетовым К в вин-но-солянокислой среде а спектрофотометре при 570 нм. [14]
Метод основан на измерении светопоглощения растворов комплекса ниобия с пирогаллолом при i 450 им. Незначительное мешающее влияние тантала и цир кония можно учесть; влияние железа устраняют, связывая его в комплекс с тиогликолевой кислотой. Молибден и титан должны быть предварительно отделены. Метод применим для анализа сплавов, содержащих 7 - 20 % ниобия. [15]
Страницы: 1 2 3 4