Комплекс - ниобий
Cтраница 4
Кислотность водно-органической среды обусловлена экстракцией в органическую фазу разных кислотно-основных форм экстракционного реагента и других лигандов. Кислотность водно-органической среды может влиять на протолитические равновесия между каталитически активными комплексами, а также частицами окислителя и восстановителя. Влияние кислотности водно-органической среды проявляется в реакции окисления о-ами-нофенола пероксидом водорода, катализируемой комплексами ниобия с а-бензоиноксимом. В результате оптимальные концентрации окислителя в разных средах различны. [46]
Образование комплекса ниобия с ЭДТА впервые зафиксировали Феррет и Мильнер [ 56 ( 123) ] в результате полярографических исследований. Кирби и Фрайзер [ 63 ( 12) ] более подробно изучали полярографическое восстановление комплекса ниобия с ЭДТА и установили, что стабильность раствора и полнота комплексообразования достигаются лишь при кипячении раствора. [47]
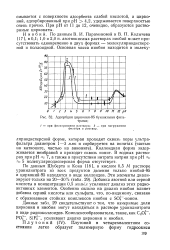 |
Адсорбция циркония-95 бумажными фильтрами. [48] |
По данным Шуберта и Кона [18], в кислом 0 5 М растворе уранилнитрата из всех продуктов деления только ниобий-95 и цирконий-95 находятся в виде коллоидов. Добавка азотной или серной кислоты в концентрации 0 5 моль / л усиливает диализ этих радиоактивных элементов. Особенно сильно на диализ ниобия влияет добавка серной кислоты или сульфата, что, по-видимому, связано с образованием стойких комплексов ниобия с 5О4 - - ионом. [49]
Этот оксид уникален, он имеет структуру, изображенную па рис. 6.1 г [8], в которой как атомы ниобия, так и кислорода образуют четыре компланарные связи, поочередно занимая позиции в одной из простейших трехмерных сеток, образованных из связанных вершинами квадратов. Альтернативно структура может быть описана как дефектная структура Nad с тремя молекулами NbO в элементарной ячейке и вакансиям. Отметим, что в структуре можно выделить и трехмерный каркас, построенный из октаэдри-ческих структурных единиц Nb6 ( Nb-Nb 2 98 А), напоминающих галогеиидные комплексы ниобия и тантала ( разд. Правильность этой модели структуры подтверждена нейтроно-графпческнм исследованием. [50]
Некоторые сложные задачи переработки тантало-ниобиевых продуктов могут быть решены на основе разработанного в Иргн-редмете под руководством автора сульфатно-пероксидного способа [41] Способ подробно изучен, испытан в полупромышленном масштабе на различных титано - и тантало-ниобиевых продуктах и внедрен в производство на нескольких предприятиях. Способ заключается в сульфатизации исходных концентратов серной кислотой при 200 - 300 С в течение 1 - 2 ч и загрузке 1 - 2 кг H2SO4 на 1 кг исходного материала. Из фильтрата нагревом его до 90 - 98 С с выдержкой при этой температуре в течение 2 - 3 ч выделяют химический концентрат, содержащий в прокаленном виде 50 - 90 % ( Nb, Та) 2О5 - Таким образом, для выщелачивания ниобия и тантала используется устойчивость растворимых перо-ксидных комплексов ниобия и тантала, а для осаждения - их способность разлагаться в горячих растворах. [51]
При этом происходит отделение ниобия и тантала также от железа, циркония и ряда других элементов. По наблюдениям авторов при непосредственном выщелачивании пиросульфатного плава окислов ниобия, тантала и титана 1 % - ным солянокислым раствором пирогаллола происходят потери ниобия вследствие образования гетерогенного комплексного суль-фатосоединения титана и ниобия. Это соединение, однако, можно разрушить подщелачиванием раствора, причем после последующего подкисле-ния оно вновь не образуется. Образованию комплекса ниобия с титаном препятствует также присутствие железа. [52]
Из водных растворов комплексного соединения алкалоиды выделяют характерно окрашенный осадок. Соединение экстрагируется спиртами, эфирами, альдегидами и кетонами. Количество ниобия находят по величине оптической плотности эфирного экстракта соединения. Предложены также методы, основанные на измерении оптической плотности водно-ацетоновых растворов рода-нидного комплекса ниобия ( см. стр. [53]
При очень высоком содержании тантала кипящий желтый раствор вскоре мутнеет и постепенно образуется желтый осадок. Осторожно добавляют еще немного таннкна и наблюдают его действие. Временное появление оранжевого оттенка, исчезающего при перемешивании, указывает на начало образования и последующего распада комплекса ниобия. Добавление таннина прекращают раньше появления неисчезающего оранжевого оттенка. Полного осаждения достигают добавлением 25 мл насыщенного раствора хлористого аммония и осторожным кипячением в течение нескольких минут. [54]
Известно [ 37, 981, что в пероксидной среде ниобий также дает окрашенный комплекс с кси-леноловым оранжевым, интенсивность окраски которого уменьшается с увеличением кислотности. Комплексов III в 0 4 N HaSO4 полностью разрушает окрашенный комплекс циркония с ксиленоловым оранжевым и не влияет на окраску комплекса ниобия. Поэтому, если раствором сравнения будет служить аликвотная часть того же раствора после добавления раствора комп-лексона III, то светопоглощение за счет комплексов ниобия и других металлов с ксиленоловым оранжевым, не реагирующих в 0 4 N HsSO4 с комплексоном III, будет полностью элиминировано. [55]
Страницы: 1 2 3 4