Комплекс - уран
Cтраница 1
Комплекс урана с аскорбиновой кислотой был использован [466] для определения содержания урана в трибутилфосфатных растворах в инертном разбавителе. При встряхивании этих растворов с водным раствором, содержащим аскорбиновую кислоту, уран переходил в водную фазу, где его определяли фотометрически. [1]
 |
Константы образования комплексов урана ( IV при 25 С. [2] |
Комплексы урана ( IV) с различными дикетонами могут быть получены осаждением из раствора или экстракцией раствором дикетона. Обычно эти комплексы слабо растворимы в воде и значительно более растворимы и неполярных органических жидкостях. Иногда они заметно летучи в вакууме. [3]
Комплекс урана ( VI) интенсивно окрашен в желтый цвет. Комплекс ванадия ( V) интенсивно окрашен в голубой цвет, а поэтому может быть использован для определения ванадия фотометрическим методом. Тартратный комплекс церия ( IV) количественно экстрагируется в присутствии избытка амина с окрашиванием неводной фазы в оранжево-красный цвет. Родий ( III) экстрагируется с интенсивным красным окрашиванием. Золото ( III) и палладий ( II) через некоторое время после экстракции восстанавливаются в оргадическом слое до металла. [4]
В комплексах урана с HRn и HFn, полученных соответственно при рН 5 2 - 5 6 и 5 0 - 5 5, наблюдаются полосы, характерные для линейной группы уранила. В случае 1ЮгРп2 полосы располагаются соответственно при 880 и 921 см-1. В отличие от молибдена комплекс W02FnCl, выделенный из концентрированной соляной кислоты, имеет широкую полосу полимерных форм около 840 см-1. [5]
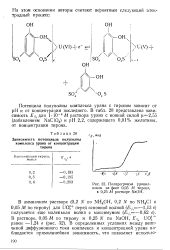 |
Полярограмма уранил-ионов на фоне 0 05 М тирона, в 0 25 М растворе NaOH. [6] |
Потенциал полуволны комплекса урана с тироном зависит от рН и от концентрации последнего. [7]
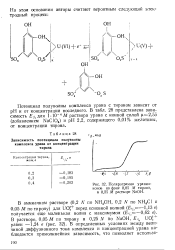 |
Полярограмма уранил-ионов на фоне 0 05 М тирона, в 0 25 Л1 растворе NaOH. [8] |
Потенциал полуволны комплекса урана с тироном зависит от рН и от концентрации последнего. В табл. 28 представлена зависимость Ец2 для Ь10 - 4Л1 раствора урана с ионной силой ц - 2 55 ( добавлением NaClO4) и рН 2 2, содержащего 0 01 % желатины, от концентрации тирона. [9]
Церковницкая и Быховцева [685] экстрагировали анионные хе-латные комплексы урана ( VI) с бензгидроксамовой кислотой и бромпирогаллоловым красным при помощи три-н-октиламина в бензоле. При использовании бензгидроксамовой кислоты экстракт разбавляли ацетоном, вводили хлорид лития ( фон), тимол в качестве поверхностно активного ( вещества и проводили полярографирование на ртутном капельном электроде. [10]
Ионообменное отделение основано на адсорбции анионных сернокислых комплексов урана сильноосновными анионообменными смолами и последующей десорбции путем вымывания ионов ура-нила, связанных в анионный комплекс, подкисленными растворами солей. [11]
Очень интересные данные были получены для комплексов урана. Быстрый обмен претерпевает также сам уран между KJU O J и ( NH JUOj O l, причем скорость-определяющей стадией при этом обмене является взаимодействие U ( IV) и U ( V), который получается в качестве промежуточного продукта реакции. [12]
Благодаря этому в осадке соотношение между комплексом урана и избыточным окрашенным органическим реагентом оказывается более благоприятным для фотометрирования, чем в исходном растворе, в который для возможно более полного связывания урана в продукт реакции приходится вводить большой избыток окрашенного реагента. На рис. 1 в общем, схематичном виде представлено влияние количества соо-садителя на полноту соосаждения комплекса урана и избыточного реагента. [13]
При изучении хлоридных, бромидных и тиоциааатаых комплексов урана ( IV) с помощью пары U4, UO2 Арланд и Ларссон [9] измерили X в зависимости от Л и общей концентрации В урана ( IV) для растворов, в которых общая концентрация 23 урана ( VI) поддерживалась высокой и постоянной. [14]
Рассмотрим, например, определение констант устойчивости комплексов урана ( VI) с уксусной кислотой. Величины, измеренные при различных рН, лежат на одной кривой, вследствие чего образованием гидроксокомплек-сов в исследованных условиях можно пренебречь. [15]
Страницы: 1 2 3 4