Наиболее прочный комплекс
Cтраница 1
Наиболее прочные комплексы с С1 - -, Вг - -, I - и SCN - ионами образует золото ( I и III), ртуть ( П) и металлы платиновой группы. Однако эти комплексы бесцветны или слабо окрашены, поэтому они не имеют прямого значения в фотометрическом анализе. Наибольшее значение в фотометрии имеют малопрочные, но интенсивно окрашенные роданидные комплексы железа ( III), кобальта ( II), молибдена ( V), вольфрама ( V), висмута, уранила и ниобия. Для фотометрического анализа применяют также образование иодидных комплексов висмута и теллура, хлоридных комплексов меди ( II) и железа ( III), а также роданидных комплексов рения и рутения. [1]
Наиболее прочные комплексы образуются с палладием и медью. Однако устойчивость комплекса с палладием превышает оптимальную величину для успешного применения реагента в качестве металлиндикатора, и титрование с применением ЭДТА в связи с этим затруднено. [2]
Наиболее прочные комплексы образуются с кислород - и фторсодержащими лигандами. [3]
Наиболее прочные комплексы торий дает с полианионными содержащими кислород лигандами, обычно когда образуются би-дентатные внутрикомплексные соединения. В качестве примеров таких реагентов, применяемых для фотометрического определения тория, можно назвать морин ( дающий в слабокислых растворах бис-комплекс), ализариновый красный S, кверцетин, хинализарин и пирокатехиновый фиолетовый. [4]
Наиболее прочные комплексы с комплексоном III образуют ионы никеля и марганца, вследствие чего они не извлекаются из раствора в его присутствии; при любом рН, а ионы кобальта, железа и цинка извлекаются. [5]
 |
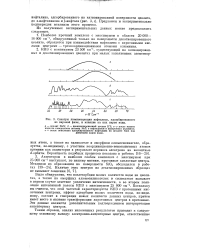
Зависимость адсорбции йода углям водного раствора ( 7 и нз паровой фазы ( 2.| Изменение поглощения йода в трепанных микрокомпонентов ( ZOK. [6] |
Наиболее прочные комплексы с йодом образуются при использовании витринита высокометаморфизованного угля ( R0 1 7 %), у него наблюдается максимальное увеличение количества парамагнитных центров при взаимодействии с йодом. Интенсивность сигнала ЭПР, а также поглощение комплекса при 296 нм возрастают при повышении концентрации йода в смеси с углем. Эти данные позволяют утверждать, что наиболее активны при взаимодействии с йодом полисопряженные структуры углей, поглощающие в ближней ИК-области спектра, при этом образуются комплексы с переносом заряда, обладающие парамагнитно активностью. [7]
Наиболее прочные комплексы возникают за счет й25 / э3 - гибридизации и внутренних u - орбиталей; они не имеют свободных внутренних rf - орбиталей и неспаренных электронов. [8]
 |
Спектры люминесценции нафталина, адсорбированного из паровой фазы, и влияние на них паров воды. [9] |
Наиболее прочный комплекс с максимумом в области 20 000 - 18 000 см 1, обнаруженный только на поверхности декатионированного цеолита, образуется при взаимодействии нафталина с апротонными кислыми центрами - трехкоординационными атомами алюминия. [10]
 |
Элементарная ячейка FeS. [11] |
Наиболее прочными комплексами Fe2, Co2 и Ni2 являются цианистые. В лабораторной практике широко используют гексацианоферрат ( П) калия K4 [ F. CN) 6 ] - ЗН2О, иног да называемый желтой кровяной солью. Кислота H4 [ Fe ( CN) 6 известна в свободном состоянии. [12]
Наиболее прочными комплексами являются дитизонаты платины, ртути, палладия, серебра, меди и висмута. Дитизонаты данных металлов окрашены в желто-оранжевый цвет и образуются в кислой среде. [13]
Наиболее прочными комплексами Fe2, Co2 и Ni2 являются цианистые. В лабораторной практике широко используют гексацианоферрат ( П) ка лия K4 [ Fe ( CN) 6 ] - ЗН2О, иног-г да называемый желтой кровяной солью. Кислота Н4 [ Ре ( СМ) б ( известна в свободном состоянии. Ион [ Ni ( CN) 4 ] 2 - имеет плоскую квад ратную структуру, rf ( Ni-С) 186 пм; d ( C-N) ИЗ пм. [14]
 |
Элементарная ячейка FeSz. [15] |
Страницы: 1 2 3 4