Наиболее прочный комплекс
Cтраница 3
Можно установить два класса акцепторов: класс А, к которому относятся металлы, образующие наиболее прочные комплексы с лигандами, донорные атомы которых являются первыми элементами каждой группы периодической системы ( N, О и F), и класс Б, включающий те металлы, которые образуют наиболее прочные комплексы с лигандами, имеющими в качестве доноров атомы второго и последующего элементов каждой группы. При этом следует указать, что металл в каждой степени окисления должен рассматриваться как самостоятельный акцептор. Большинство металлов с пустыми или полностью заполненными ( п - 1) 2-орбиталями принадлежат к классу А, так же как и переходный элемент, у атома которого имеется один, два или три d - электрона. К классу Б относится лишь незначительное число металлов. Почти все переходные элементы занимают промежуточное положение. [31]
О и F), и класс В, включающий те металлы, которые образуют наиболее прочные комплексы с лигандами, имеющими в качестве доноров атомы второго и последующего элементов каждой группы. При этом следует указать, что металл в каждой степени окисления должен рассматриваться как самостоятельный акцептор. [32]
Можно установить два класса акцепторов: класс А, к которому относятся металлы, образующие наиболее прочные комплексы с лигандами, донорные атомы которых являются первыми элементами каждой группы периодической системы ( N, О и F), и класс Б, включающий те металлы, которые образуют наиболее прочные комплексы с лигандами, имеющими в качестве доноров атомы второго и последующего элементов каждой группы. При этом следует указать, что металл в каждой степени окисления должен рассматриваться как самостоятельный акцептор. Большинство металлов с пустыми или полностью заполненными ( п - 1) й-орбиталями принадлежат к классу А, так же как и переходный элемент, у атома которого имеется один, два или три d - электрона. К классу Б относится лишь незначительное число металлов. Почти все переходные элементы занимают промежуточное положение. [33]
Можно установить два класса акцепторов: класс А, к которому относятся металлы, образующие наиболее прочные комплексы с лигандами, донорные атомы которых являются первыми элементами каждой группы периодической системы ( N, О и F), и класс Б, включающий те металлы, которые образуют наиболее прочные комплексы с лигандами, имеющими в качестве доноров атомы второго и последующего элементов каждой группы. При этом следует указать, что металл в каждой степени окисления должен рассматриваться как самостоятельный акцептор. Большинство металлов с пустыми или полностью заполненными ( п - 1) с ( - орбиталями принадлежат к классу А, так же как и переходный элемент, у атома которого имеется один, два или три d - электрона. К классу Б относится лишь незначительное число металлов. Почти все переходные элементы занимают промежуточное положение. [34]
Например, установлено, что катионы, особенно чувствительные к стабилизации в поле лигандов, образуют наиболее прочные комплексы с донор-ными атомами, которые обусловливают большие расщепления в поле лигандов, и наоборот. [35]
Например, установлено, что катионы, особенно чувствительные к стабилизации в поле лигандов, образуют наиболее прочные комплексы с донор-ными атомами, которые обусловливают большие расщепления в поле лигандов, и наоборот. [36]
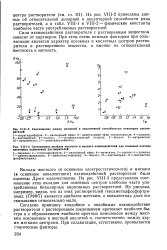 |
Соотношение между донорной и акцепторной способностью некоторых растворителей.| Соотношение вкладов жесткого и мягкого взаимодействий для основных центров некоторых апротонных растворителей. [37] |
Согласно принципу подобное с подобным взаимодействие растворителя с растворенным соединением протекает наиболее быстро и с образованием наиболее прочных комплексов между жестким основанием и жесткой кислотой и, соответственно, между двумя мягкими центрами. При сольватации, естественно, проявляются стерические факторы. [38]
Все металлы-комплексообразователи можно разделить на два класса: класс А, к которому относятся металлы, образующие наиболее прочные комплексы с лигандами, донорные атомы которых являются первыми элементами каждой группы периодической системы ( N, О и F), и класс Б, включающий те металлы, которые образуют наиболее прочные комплексы с лигандами, имеющими в качестве доноров атомы второго и последующего элементов каждой группы. [39]
Именно поэтому ион Fe ( III) весьма мало похож на ионы других переходных металлов и именно поэтому он образует свои наиболее прочные комплексы с анионными, а не с содержащими азот лигандами. [40]
Различные валентные состояния металла часто отличаются по стереохимии, экстракционному поведению и другим свойствам их комплексов, а также по типам лигандов, с которыми они образуют наиболее прочные комплексы. В таких случаях в качестве основы высокоизбирательных аналитических методов можно использовать экстракцию ( предпочтительно), ионный обмен, осаждение или некоторые другие приемы с последующим окислением или восстановлением и взаимодействием с соответствующим лигандом. [41]
 |
Структура комплекса брома с 1 4-диокса-ном. [42] |
Для наиболее слабых комплексов, например комплекса 1 4-диоксана с хлором, ДА-связь по длине ближе к сумме вандер-ваальсовых радиусов, чем к сумме ковалентных радиусов, а для наиболее прочных комплексов галогенов с аминами, пиридином и селеносодержащими донорами длина ДА-связи лишь на 0 1 - 0 3 А больше суммы ковалентных радиусов. [43]
Щелочные и щелочноземельные металлы образуют наиболее прочные комплексы с оксо-анионами, переходные металлы - с N - co держащими и в меньшей степени с S - co держащими соединениями, такие металлы, как Zn и Hg, образуют наиболее прочные комплексы с тио-соединениями. [44]
Согласно современным представлениям координационной химии, ионы, распределение электронов в которых близко к распределению электронов в атомах инертных газов ( щелочные и щелочноземельные металлы, титан, цирконий, гафний, алюминий, скандий), склонны к образованию наиболее прочных комплексов с лигандами, содержащими в качестве доноров атомы кислорода, в том числе с [ 3-дикетонами. Это же свойство проявляют также ионы лантаноидов и актиноидов. [45]
Страницы: 1 2 3 4