Фиолетовый комплекс
Cтраница 1
Фиолетовый комплекс, устойчивый в кислой среде, используют для фотоколориметрического определения железа ( Ш) в присутствии железа ( П), а также для косвенного определения фторидов ( см. стр. Этот метод малочувствителен, молярный коэффициент погашения равен 2 6 - 103 при Хмако 490 нм. [1]
Интенсивность окраски соответствующего фиолетового комплекса марган-ца ( Ш) с ортофосфорной кислотой [71] составляет 60 % интенсивности окраски пирофосфатного комплекса. Молярный коэффициент погашения пирофосфатного комплекса равен - 8 0 - 102 при А макс - 520 нм. При растворении окислов марганца в горячей ортофосфориой кислоте образуется окрашенный комплекс, в котором часть марганца имеет валентность выше двух. [2]
Метод основан на образовании фиолетового комплекса при взаимодействии иона SbCle с кристаллическим фиолетовым в солянокислой среде и экстракции образовавшегося соединения толуолом. [3]
Метод основан на образовании фиолетового комплекса при взаимодействии иона ( 8ЬС16) - с кристаллическим фиолетовым и экстракции образовавшегося соединения толуолом. [4]
Определение основано на образовании фиолетового комплекса при взаимодействии меди ( II) с дитизоном в слабокислой среде. Максимальное поглощение лучей окрашенным соединением наблюдается около 510 ммк. Определению меди мешают все ионы тяжелых металлов, реагирующие с дитизоном. [5]
Согласно этим данным, в фиолетовом комплексе атомы железа образуют треугольник, к каждой стороне плоскости которого, образованной этими атомами, присоединяется по одной молекуле дифенилацетилена. Что касается структуры Feg ( CO) l2, установленной Далем [176, 47], то фиолетовый комплекс ( C6H5CCCeH5) 2Fe3 ( CO) 8 можно рассматривать как додекакарбонил железа, две СО-группы которого замещены дифенилацетиленом. [6]
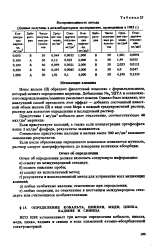 |
Воспроизводимость метода ( Данные получены в межлабораторном эксперименте, проведенном 1982 г. [7] |
Ионы железа ( П) образуют фиолетовый комплекс с формальдоксимом, который мешает определению марганца. Добавление Na4 ЭДТА и солянокислого гидроксиламина / аммиака уменьшает помехи. Однако было показано, что наилучший способ преодолеть этот эффект - добавить постоянный известный объем железа ( П) в виде соли Мора в - а-ждий градуировочный раствор, раствор для холостого определения и исследуемый раствор. [8]
 |
Воспроизводимость метода по ИСО 6333. [9] |
Ионы железа ( II) образуют фиолетовый комплекс с формальдокси-мом, который мешает определению марганца. Добавление N34 ЭДТА и солянокислого гидроксиламина / аммиака уменьшает помехи. Однако было показано, что наилучший способ преодолеть этот эффект - добавить постоянный известный объем железа ( II) в виде соли Мора в каждый градуировочный раствор, раствор для холостого определения и исследуемый раствор. [10]
В кипящем бензоле или легком керосине фиолетовый комплекс перегруппировывается в более устойчивый черный изомер. Рентгеноструктурное исследование строения этих двух комплексов показало, что в фиолетовом изомере молекулы PhC CPh не комбинируются и расположены на противоположных сторонах треугольника из атомов железа [43], в то время как в черном изомере молекулы ацетилена конденсированы и образуют фер-рациклопентадиеновое кольцо. [11]
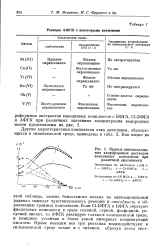 |
Кривые светопоглоще. [12] |
Если С1 - БФГА и БФГА образуют фиолетовые комплексы в среде соляной, серной, фосфорной, уксусной кислот, то АФГК реагирует только в солянокислой среде, и комплекс устойчив в более узком интервале концентраций кислоты. [13]
Как уже указывалось, железо при рН2 образует фиолетовый комплекс с салициловой кислотой и повышением рН до 3 способствует его более полному связыванию. Однако в присутствии меди настолько уменьшить концентрацию ионов водорода нельзя, так как при этом она образует желтый салицилатный комплекс CuSal. Лишь при рН 2 5 ионы меди не образуют окрашенного комплекса, а железо практически полностью связывается. [14]
Как уже указывалось, железо при рН 2 образует фиолетовый комплекс с салициловой кислотой и повышение рН до 3 способствует более полному связыванию железа. [15]
Страницы: 1 2 3 4