Фиолетовый комплекс
Cтраница 2
Эриохромцианин дает с галлием при рН 4 2 ( ацетатный буфер) фиолетовый комплекс состава 1: 2 [38, 1279], с максимумом светопоглощения при X 540 нм. [16]
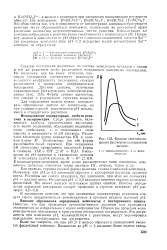 |
Кривые светопогло. [17] |
Выше мы говорили, что при рН 2 железо образует с салициловой кислотой фиолетовый комплекс. [18]
 |
Число молекул воды, гидратирующих различные ионы при 25. [19] |
Связанные в комплекс молекулы воды во многих случаях присоединяются очень прочно ( даже в фиолетовом комплексе [ Сг ( Н2О) 6 ] С13) и при комнатной температуре не удаляются в вакууме над серной кислотой; только при температурах около 200 и выше начинается глубоко идущее разложение. [20]
Особенность этого метода в том, что он позволяет удобно исследовать промежуточные соединения реакции, например фиолетовый комплекс Ре820з, образующийся при реакции ионов Fe ( III) с ионами тиосульфата. [21]
Арсеназо I, водные растворы которого окрашены в красный цвет, в солянокислых растворах образует с цирконием и гафнием фиолетовые комплексы. [22]
Предложенный в [1115] Спектрофотометрический метод определения NH2OH основан на образовании в щелочной среде ( рН 8 - 12) фиолетового комплекса в присутствии V5 и триэтаноламина. [23]
Метод основан на цветной реакции индия с дифенилка базоном при рН Г () - 6 0, при которой образуется фиолетовый комплекс. В отсутствие индия раствор остается буровато-желтым. Железо и медь маскируются тио-мочевиной. В присутствии больших количеств этих элементов индий отделяют экстракцией эфиром из бромистоводородной кислоты. [24]
Комплексонометрический метод Ионы хрома ( III) медленно взаимодействуют с комплексоном III при кипячении в слабокислой среде ( рН 5 3 - 6) с образованием интенсивно окрашенного фиолетового комплекса. Окраска комплекса мешает определению точки эквивалентности. [25]
Механизм этой реакции подобен механизму реакции хрома ( У1) с дифенилкарбазидом ( см. стр. Фиолетовый комплекс рения экстрагируется хлороформом. Молярный коэффициент погашения составляет 2 04 - 10 при Ямакс - - 545 нм. [26]
Основные условия определения Реактив взаимодействует с железом с очень высокой чувствительностью - - 0 025 MKt / мл. Фиолетовый комплекс трехвалентного железа с реактивом спектрофотометрируют при 530 нм. [27]
Разбавленным раствором аммиака доводят рН раствора до - 2 0 по универсальному индикатору и осаждают висмут свежеприготовленным раствором купферона. НОГО раствора салициловой кислоты ( образуется фиолетовый комплекс с железом ( Ш), 8 твм восстанавливавт железо, прибавляя 1 -ный раствор аскорбиновой кислоты до обесцвечивания раствора л сверх того еще 1 - 2 мл. [28]
Серебряные комплексы аминокислот представляют только исторический интерес, так как с их помощью были открыты и впервые определены гексоновые основания. Описаны также красные комплексы с хромом и фиолетовые комплексы с кобальтом. [29]
Стабильный красный комплекс состава 2: 1 с максимумом светопоглощения 548 нм образуется в разбавленном растворе соли кальция. В присутствии больших количеств кальция возникает значительно менее стабильный фиолетовый комплекс состава 1: 1 с максимумом светопоглощения 750 нм. [30]
Страницы: 1 2 3 4