Низкоспиновый комплекс
Cтраница 1
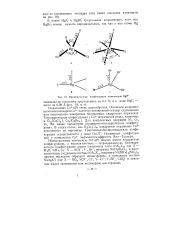 |
Промежуточные конфигурации комплексов Hga. [1] |
Низкоспиновые комплексы Ni2 ( d8) обычно имеют квадратную конфигурацию, а высокоспиновые - тетраэдрическую. Октаэдри-ческую конфигурацию имеют соединения типа NiA2X2, где А - Н2О, МНз, ру; X - SCN, I, Вг -, например Ni ( H2O) 2Cl2, и высокоспиновые соединения состава NiA4X2, например Ni ( NHs) 4 ( NO2) 2, причем последние образуют транс-формы, а комплексы состава Nien2XY ( где X - NO2, SCN -, Cl -; Y-СГ, l -, BF, СЮ) в основном имеют мономерное или полимерное ц с-строение. [2]
Низкоспиновые комплексы являются наиболее устойчивыми, что объясняется проникновением двух ( для к. [3]
Низкоспиновый комплекс образуется лишь в том случае, когда в пятом и шестом положениях находятся группы, расположенные справа в спектрохимическом ряду. Так, в низкоспиновом ферроцитохроме с пятое и шестое координационные положения занимает азот имидазольных групп гистидиновых остатков. При физиологических условиях ферро-цитохром с не может связывать кислород, окись углерода, фтор или циа-нид. Окисленный ферроцитохром с также является низкоспиновым. Миоглобин и гемоглобин представляют собой высокоспиновые комплексы ферро-иона с имидазольной группой гистидина в пятом положении и молекулой воды в шестом. Полный магнитный момент молекулы оксигемоглобина становится равным нулю. Комплекс ферро-иона со спаренными спинами дает темно-красную окраску благодаря поглощению, связанному в основном с порфириновым кольцом. Окисление этих двух белков кислородом протекает сравнительно медленно, несмотря на то, что термодинамически это выгодно. Частично это связано с тем, что каждый такой процесс происходит с изменением спинового числа. При использовании других окисляющих агентов получаются высокоспиновые комплексы ферри-иона с белками, называемые метмиоглобином или метгемоглобином. [4]
Низкоспиновые комплексы являются наиболее устойчивыми, что объясняется проникновением двух ( для к. [5]
Низкоспиновые комплексы кобальта ( П) имеют две дырки в dxj) 2 и одну в й 2-орбиталях. [6]
Низкоспиновые комплексы двухвалентного кобальта с координационным числом четыре всегда имеют плоскую квадратную конфигурацию. Типичными примерами являются комплексы малеоди-нитрилдитиолата кобальта [ NR4 ] 2 [ Co ( S2C2 ( CN) 2) 2 ] ( 14) и комплекс дитиоацетилацетона кобальта Co ( sacsac) 2 ( 15) [34]; в обоих случаях атом кобальта связан с четырьмя атомами серы, которые образуют плоское квадратное окружение. [7]
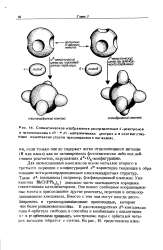 |
Схематическое изображение распределения rf - эпектронов в низкоспиновых ds - и rf6 металлических центрах и в соответствующих комплексах ( после присоединения лигандов. [8] |
Для низкоспиновых комплексов ионов металлов второго и третьего периодов с конфигурацией ds характерна тенденция к образованию четырехкоординационных плоскоквадратных структур Такие ds - комплексы [ например, фосфинродиевый комплекс Уил-кинсона RhCl ( PPh3) 3 ] довольно часто оказываются хорошими гомогенными катализаторами Они имеют свободные координационные места и присоединяют другие реагенты, переходя в пятикоор-динационные комплексы. [9]
В низкоспиновом комплексе [ Co ( NH3) J3 A0 значительно больше, чем в [ CoFeJ3 -, поэтому все оставшиеся электроны располагаются на несвязывающих ( dxy, dX2, dl / z) орбиталях, что обусловливает повышенную устойчивость комплекса. [10]
 |
Энергетические характеристики ионов комплексообраэоаателеи в октаэдрическом поле миандов. [11] |
В низкоспиновых комплексах ион Со3 ( if1) имеет J-электроны только на слабо экранирующих ядро низкоэнергетических - орбиталях, благодаря этому такие комплексы Со3 весьма прочны и их известно очень много. [12]
 |
Распределение d - электронов в комплексах db в слабом ( а и сильном ( б кристаллических полях. [13] |
В низкоспиновых комплексах до шести электронов иона металла располагаются на орбиталях, ориентированных в направлении между лигандами, а орбитали dz и dx - y остаются пустыми и могут участвовать в связях, принимая электронную плотность от лигандов. [14]
В низкоспиновом комплексе все пять электронов иона металла располагаются на орбиталях, ориентированных в направле ниях между лигандами, а орбитали dz - и rf остаются пустыми. Они могут участвовать в связях и принимать электронную плотность от лигандов. [15]
Страницы: 1 2 3 4