Салицилатной комплекс
Cтраница 1
 |
Спектры поглощения сали-цилатных комплексов. [1] |
Салицилатные комплексы Со ( II) и А1 в интервале от 360 до 750 нм света не поглощают и определению Ti и Fe не мешают. Салицилатные комплексы Ti ( IV) и Fe ( III) при рН - 4 образуются практически мгновенно и устойчивы в течение длительного времени. [2]
По исследованию салицилатных комплексов железа и меди различными методами имеется обширная литература. [3]
Высокая устойчивость цитратных и салицилатных комплексов ( см. табл. 5.4) обусловлена образованием хелатных циклов, в которых ион металла оказывается заключенным в ионно-ковалентные клешни, которые пространственно экранируют ион металла и координационные химические связи от разрушительной атаки молекул растворителя. [4]
В растворах аммиачного и салицилатного комплекса поляризация имеет в основном концентрационный характер, причем в последнем случае она осложняется образованием пассивной пленки на катоде. [5]
Если константы диссоциации этих салицилатных комплексов не известны, то их относительную прочность нетрудно определить простым опытом. Если смешать растворы солей железа и меди и прибавить к смеси недостаточное количество салицилата ( так, чтобы его не хватало для связывания обоих ионов, Си2 и Fe3), то возникает фиолетовая окраска раствора. [6]
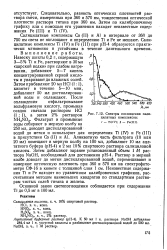
Из рассмотрения спектров поглощения салицилатных комплексов титана и железа ( рис. 7.12) видно, что наиболее целесообразно фотометрирование раствора смеси проводить при 360 и 570 нм. [7]
 |
Спектры поглощения салицилатных комплексов. / - раствор титана. 2 - раствор железа. [8] |
Из рассмотрения спектров поглощения салицилатных комплексов титана и железа ( рис. 11.5) видно, что наиболее целесообразно фотометрирование раствора смеси проводить при 360 и 570 нм. При 570 нм светопоглощение салицилатного комплекса Fe точно такое же, как и при 360 нм, но светопоглощение са-лицилата титана отсутствует. Следовательно, разность оптических плотностей раствора смеси, измеренных при 360 и 570 нм, тождественна оптической плотности раствора титана при 360 нм. [9]
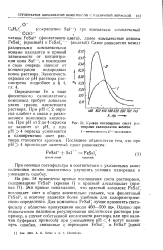 |
Кривая поглощения света растворами салицилатов железа. [10] |
Определение Fe в виде фиолетового салицилатного комплекса требует довольно узких границ кислотности раствора. При рН 2 окраска слабеет в связи с разложением комплекса кислотами. При рН от 2 до 4 окраска не зависит от рН, а при рН 4 окраска усиливается и одновременно цвет раствора становится красным. [11]
Из рассмотрения спектров поглощения салицилатных комплексов титана и железа ( рис. 7.12) видно, что наиболее целесообразно фотометрирование раствора смеси проводить при 360 и 570 нм. [12]
Обнаружению иона Fe3 в виде салицилатного комплекса практически не мешает ни один катион. К 3 - 5 каплям исследуемого раствора добавляют равное количество раствора салициловой кислоты. При установлении по универсальному индикатору значения рН - 2 появляется буро-фиолетовое окрашивание. Появление желтого окрашивания указывает на присутствие ионов железа. [13]
Для определения обратимости процесса восстановления кадмия из салицилатного комплекса были сняты полярограммы растворов с постоянной концентрацией салицилата 0 128 М и различными концентрациями соли кадмия. [14]
Целью настоящей работы является выяснение возможности образования салицилатных комплексов кадмия, свинца и цинка, а также определение констант нестойкости этих соединений. [15]
Страницы: 1 2 3 4