Салицилатной комплекс
Cтраница 4
Так, степень связывания Fe3 в роданидный комплекс заметно уменьшается в присутствии С1 -, а при наличии фосфорной кислоты происходит полное обесцвечивание раствора роданида железа. Между тем большое количество С1 - совершенно не влияет на определение железа в виде более прочного салицилатного комплекса; очень мало сказывается также присутствие фосфорной кислоты и фосфатов. Поэтому реактивы для фотометрирования необходимо выбирать таким образом, чтобы окрашенное соединение определяемого иона было достаточно устойчивым ( К sg 1 - 10 8) и значительно более прочным, чем возможные соединения этого иона с другими компонентами, присутствующими в растворе. [46]
Чем прочнее окрашенный комплекс, тем меньше влияют на определение многие присутствующие в растворе посторонние ионы. Так, например, степень связывания железа в роданидный комплекс заметно уменьшается в присутствии ионов хлора, а при наличии фосфорной кислоты происходит даже полное обесцвечивание раствора роданида железа. Между тем присутствие большого количества хлоридов совершенно не влияет на определение железа в виде значительно более прочного салицилатного комплекса, очень мало сказывается также присутствие фосфатов. [47]
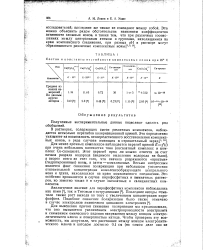 |
Состав и константы нестойкости комплексных ионов при 25 С. [48] |
Этот перегиб вряд ли можно отнести за счет начала разряда водорода ( видимого выделения водорода не было), а скорее всего за счет того, что сначала разряжаются простые ( гидратированные) ионы, а затем - комплексные. Весьма интересным является факт снижения поляризации при небольшом увеличении относительной концентрации комплексообразующего центрального иона и групп, находящихся на краю комплексного соединения. Это особенно проявляется в случае пирофосфатных и аммиачных растворов, но заметно также и в случае оксалатных и салицилатных комплексов. [49]
Салициловая кислота относится к слабым кислотам ( Kn2sa - 10 - 3, / Сн2за1 Ю-13), поэтому при рН 1 8 - 2 5 образуется только моносалицилатный комплекс железа, который при увеличении кислотности разрушается. Повышение рН раствора, наоборот, увеличивает относительную концентрацию анионов салициловой кислоты, что в свою очередь приводит к образованию комплексов железа с большим координационным числом. Спектры поглощения всех трех комплексов сильно отличаются между собой. Вследствие этого при определении железа в виде салицилатного комплекса необходимо придерживаться определенной кислотности раствора. [50]
Прочность окрашенного соединения и его устойчивость в водных растворах увеличиваются с возрастанием констант устойчивости. Чем выше прочность окрашенного комплекса MRn, тем полнее определяемый ион М связывается с фотометрическим реагентом R в окрашенное соединение, тем выше могут быть точность и чувствительность фотометрического определения, меньше влияние посторонних ионов, присутствующих в растворе. Так, степень связывания Fe ( III) в роданидный комплекс заметно уменьшается в присутствии хлорид-ионов, а при наличии фосфорной кислоты происходит полное обесцвечивание раствора роданида железа. Между тем большие количества хлорид-ионов практически не влияют на определение Fe ( III) в виде более прочного салицилатного комплекса; в значительно меньшей степени сказывается также присутствие фосфорной кислоты и фосфат-ионов. Поэтому реагенты для фотометрического анализа необходимо выбирать таким образом, чтобы окрашенное соединение определяемого иона было бы достаточно устойчивым и значительно более прочным, чем возможные соединения этого реагента с другими ионами, содержащимися в анализируемом растворе. При этом следует иметь в виду, что для количественной оценки образования окрашенного соединения определяемого иона термодинамические или концентрационные константы в обычном виде можно использовать лишь при отсутствии побочных реакций. [51]
Прочность окрашенного соединения и его устойчивость в водных растворах увеличиваются с возрастанием констант устойчивости. Чем выше прочность окрашенного комплекса MRn, тем полнее определяемый ион М связывается с фотометрическим реагентом R в окрашенное соединение, тем выше могут быть точность и чувствительность фотометрического определения, меньше влияние посторонних ионов, присутствующих в растворе. Так, степень связывания Fe ( III) в роданидный комплекс заметно уменьшается в присутствии хлор-ионов, а при наличии фосфорной кислоты происходит полное обесцвечивание раствора роданида железа. Между тем, большие количества хлор-ионов практически не влияют на определение Fe ( III) в виде более прочного салицилатного комплекса; в значительно меньшей степени сказывается также присутствие фосфорной кислоты и фосфат-ионов. Поэтому реагенты для фотометрического анализа необходимо выбирать таким образом, чтобы окрашенное соединение определяемого иона было бы достаточно устойчивым и значительно более прочным, чем возможные соединения этого реагента с другими ионами, содержащимися в анализируемом растворе. При этом следует иметь в виду, что для количественной оценки образования окрашенного соединения определяемого иона термодинамические или концентрационные константы в обычном виде можно использовать лишь при отсутствии побочных реакций. [52]
Прочность окрашенного соединения и его устойчивость в водных растворах увеличиваются с возрастанием констант устойчивости. Чем выше прочность окрашенного комплекса MRn, тем полнее определяемый ион М связывается с фотометрическим реагентом R в окрашенное соединение, тем выше могут быть точность и чувствительность фотометрического определения, меньше влияние посторонних ионов, присутствующих в растворе. Так, степень связывания Fe ( III) в роданидный комплекс заметно уменьшается в присутствии хлор-ионов, а при наличии фосфорной кислоты происходит полное обесцвечивание раствора роданида железа. Между тем, большие количества хлор-ионов практически не влияют на определение Fe ( III) в виде более прочного салицилатного комплекса; в значительно меньшей степени сказывается также присутствие фосфорной кислоты и фосфат-ионов. Поэтому реагенты для фотометрического анализа необходимо выбирать таким образом, - чтобы окрашенное соединение определяемого иона было бы достаточно устойчивым и значительно более прочным, чем возможные соединения этого реагента с другими ионами, содержащимися в анализируемом растворе. При этом следует иметь в виду, что для количественной оценки образования окрашенного соединения определяемого иона термодинамические или концентрационные константы в обычном виде можно использовать лишь при отсутствии побочных реакций. [53]
Страницы: 1 2 3 4