Шестикоординационный комплекс
Cтраница 2
Многие металлы образуют почти исключительно шестикоординационные комплексы. Именно результаты изучения этой большой серии октаэдрических комплексов Сг111 и Со1 позволили А. [16]
Известно большое число примеров оптически активных шестикоординационных комплексов металлов. Для выделения энантиомеров используют такие же методы, как и для органических соединений; для обнаружения оптической активности комплексов используются те же приборы, что и для органических соединений. [18]
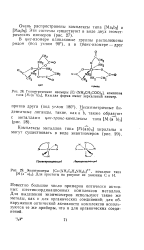
В противоположность системам с координационным числом четыре шестикоординационные комплексы дают много примеров оптической изомерии; очень часто они встречаются среди соединений или ионов типа [ М ( АА) з ], например оптические изомеры триоксалатного комплекса xpoMa ( III), XVIII и XIX. Бидентатные лиганды обычно содержат атом углерода, но известны по крайней мере три оптически активных, чисто неорганических комплекса. Один из них был приготовлен Вернером для доказательства того, что оптическая активность этих систем обусловлена не атомом углерода. [19]
В работах [5, 31, 47, 50, 53] проведено исследование спектров ЯКР шестикоординационных комплексов хлористого олова с кислородсодержащими донорами. Как уже обсуждалось, характер расщепления спектров может дать сведения о геометрическом строении комплексов. Сопоставлением характера расщепления в спектрах 36С1 SnCl4 - 2D ( рис. 7 - 7) с предполагаемой схемой расщепления для цис - и / прайс-изомеров ( рис. 7 - 1) в работе [5] было установлено строение ряда октаэдр ических комплексов. Так, комплексы SnCl4 - 2C2H5OH, 5пС14 - 2РОС13 и SnCl4 - CeH5NO2 были отнесены к цыс-изомерам. [20]
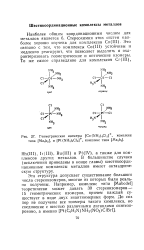 |
Геометрические изомеры [ Со ( NH3 4C12 ], комплекс типа [ Ма4Ь2 ], и [ Pt ( NH3 3C13 ], комплекс типа [ Ма3Ь3 ]. [21] |
В большинстве случаев ( исключения приведены в конце главы) Шестикоординационные комплексы металлов имеют октаэдриче-скую структуру. [22]
Данные о межатомных расстояниях и валентных углах при атоме металла в исследованных шестикоординационных комплексах и для сравнения в нескольких четырехкоординационных ( плоскостных) комплексах переходных металлов с родственными лигандами приведены в табл. 44, из которой видно, что параметры металлоциклов во всех случаях довольно близки друг к другу. [23]
Для плоских квадратных комплексов не представляется возможным успешно применить широко разработанное для шестикоординационных комплексов обобщение об отношении заряда к радиусу. Скорость обмена С1 в [ АиСЦ ] на С1 - примерно в 10 раз больше, чем для [ PtCUl, хотя по величине заряда ионов металлов можно было ожидать обратный порядок. [24]
Исследование гликолятных комплексов гадолиния [ ЗЗа ] показало, что хотя в растворе присутствует шестикоординационный комплекс Gd ( HOCH2C02) j -, в фазе ионита можно обнаружить лишь четырехкоорди-национный комплекс. Существуют также другие аналогичные случаи, связанные, вероятно, со стерическими затруднениями, а также с неблагоприятными электростатическими условиями для взаимодействия аниона-лиганда с низшим анионным комплексом в фазе ионита, который представляет собой среду с относительно низкой диэлектрической постоянной. [25]
Активированный комплекс образуется за счет присоединения к аммиакату двух ионов НОГ ( щелочная среда): двухвалентная медь способна давать шестикоординационные комплексы. Образовавшийся комплекс непрочен и быстро разлагается; разрыв связей идет так, как указано чертой. [26]
Авторы работы [31] показали, что электронный спектр никеля в другом комплексе - Ni ( NO3) 4 - - характерен для шестикоординационного комплекса, а некоторые из нитратных групп могут быть бидентатными. [27]
Он отметил, что в Т - форме может быть только блок, в котором вокруг железа координировано пять ли-гандов, тогда как шестикоординационные комплексы независимо ют валентности и спинового состояния железа существуют в Т - - форме. Он предположил, что конформационный переход белка запускается просто присоединением шестого лиганда. Процесс может осуществляться или путем вытеснения какой-то группы, блокирующей место расположения лиганда, или путем образования водородной связи с дистальным гистидином. [28]
Гидрирование родиевого комплекса, включающего четырехкоордина-ционный атом родия, связанный с двумя молекулами фосфина, одной молекулой растворителя и атомом хлора, приводит к шестикоординационному комплексу, содержащему два атома водорода. Этот комплекс может связывать молекулы растворителя с образованием промежуточного соединения с участием rf - орбиталей металла. [29]
Тетрагидрофуран, будучи значительно более основным, чем эфир, способен образовывать как лиганд достаточно прочные связи с хромом ( III) и поэтому он стабилизирует трифенилхромовое соединение в виде октаэдрического шестикоординационного комплекса. Диэтиловый эфир же не координируется, и действительно, он разрушает твердый тетрагидрофуранат в результате вымывания тетрагидрофурана. Тетрагидрофурановые растворы трифенилхрома, однако, более стабильны и без заметного разложения выдерживают значительное разбавление диэтиловым эфиром. [30]
Страницы: 1 2 3 4