Плоский комплекс
Cтраница 3
Наконец, борный ангидрид В2О3 характеризуется слоистой структурой, в которой все плоские комплексы ВО3 имеют только общие для двух атомов бора атомы кислорода. [31]
Так как имеются убедительные доказательства того, что маршрут реакций замещения в плоских комплексах с участием растворителя включает прямое ассоциативное замещение растворителем, следует ожидать, что вклад этого маршрута в общую скорость реакции должен повышаться с увеличением координационной способности растворителя. [32]
Такое допущение, справедливое для чистых состояний Cu ( II) в квадратных плоских комплексах, может оказаться неверным при искажениях комплексов, вследствие чего волновая функция неспаренного электрона может содержать примеси других состояний. Теория не предусматривает также образования химических связей с аксиальными лигандами, что вряд ли справедливо в случае оксидных стекол. [33]
В работе [3] мы сделали попытку применить результаты теории МО, развитой для квадратных плоских комплексов Cu ( II) [5, 6] и комплексов ванадила симметрии Cit [2, 7], для оценки распределения спиновой плотности между центральным атомом и кислородными лигандами в оксидных стеклах. Как было отмечено выше, полученные нами экспериментальные результаты не противоречат исходным положениям этой теории. Вместе с тем автоматический перенос результатов работ [2-7 ] на изученные нами объекты сохраняет все недостатки, присущие данной теории, и привносит некоторые новые, связанные со спецификой оксидных стекол по сравнению с рассмотренными в теории примерами замороженных органических растворов. [34]
Не существует, однако, причины, по которой перенос заряда, необходимый для плоских комплексов, будет возможен в сколько-нибудь меньшей степени, чем соответствующие состояния тетраэдрических молекул. [36]
Рассмотрим теперь схему расщепления - уровней в тетрагонально искаженных октаэдрических, а также в плоских комплексах. [37]
Обсудите доказательство того, что константа ki в выражении для скорости реакции замещения в квадратных плоских комплексах связана с бимолекулярным сольволизом. [38]
Музыкантовой, посвященная развитию и прямому экспериментальному подтверждению высказанного А. А. Гринбергом предположения, что механизм окисления плоских комплексов платины ( П) сводится к промежуточному присоединению окислителя к комплексу по 3 - й координате. [39]
Важность такого типа экспериментов состоит в том, что они позволяют исключить другие возможные механизмы [76] для плоских комплексов с квадратно-пирамидальными пятикоординированными интермедиатами. Такая структура обычна для комплексов с КЧ 5, хотя определенно доказанных примеров такой структуры для Pt ( II) не имеется. На рис. 5.17 показаны возможные схемы реакций с квадратно-пирамидальным интермедиа-том. [40]
Кристаллы K2Ni ( CN) 4 и K2Ni ( CN) 4 - H20 изоморфны; они содержат плоские комплексы Ni ( CN) 42 - и являются диамагнитными. Многие другие комплексы никеля, плоское строение которых в ряде случаев доказано методом дифракции рентгеновских лучей, удовлетворяют этому магнитному критерию. Все соединения палладия ( П) и платины ( П) диамагнитны. [41]
Кинетические данные для реакции (5.22) показывают, что эти реакции описываются уравнением с двумя членами, напоминая реакции плоских комплексов. Однако в случае Pt ( QAS) X это уравнение характеризуется изменением ki с изменением реагента. Это поведение можно объяснить тем [74], что в метаноле происходит интенсивное образование ионных пар между реагирующими соединениями. [42]
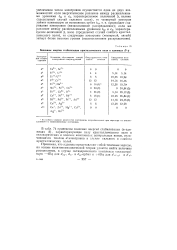 |
Величины энергии стабилизации кристаллического поля в единицах D q. [43] |
В табл. 74 приведены значения энергий стабилизации ( в единицах А), характеризующие силу кристаллического поля в октаэдрических и плоских комплексах центральных ионов, отличающихся числом rf - электронов в случае сильного и слабого кристаллических полей. [44]
 |
Цвет и расстояния Me-Me в комплексах платины. [45] |
Страницы: 1 2 3 4
