Критический комплекс
Cтраница 2
Физический смысл фактора активности F вытекает из представления об образовании реагирующими ионами продукта присоединения - так называемого критического комплекса, который, согласно Бренстеду, мономолекулярно распадается на конечные продукты. Скорость реакции зависит от скорости распада критического комплекса. [16]
Далее Скэтчард отмечает, что разница между его подходом и подходом Лейдлера и Эйринга заключается в разнице моделей критического комплекса. В модели Скэтчарда рассматриваются две сферы, причем каждая имеет заряд одного из исходных ионов, и эти заряды симметрично распределены вокруг каждого центра. В модели Лейдлера и Эйринга рассматривается одна сфера, причем суммарный заряд симметрично распределен вокруг ее центра. Эти две модели представляют собой два предельных случая как по структуре, так и по распределению заряда. [17]
Энергию, которая необходима для выталкивания трех атомов водорода из их положений в стабильном метилгалогениде в плоскую конфигурацию критического комплекса, можно оценить, исходя из силовых постоянных деформационных колебаний [24] и межъядерных расстояний. Из данных табл. 8.20 видно, что эта энергия достаточно велика и составляет примерно постоянную долю от наблюдаемой энергии активации. [19]
Следует подчеркнуть, что принятая нами энергетическая картина является чрезвычайно грубой, поскольку в соответствии с известной теорией критического комплекса химической кинетики в действительности переходными состояниями являются критические комплексы, имеющие более низкие энергосодержания, чем рассматриваемые нами переходные состояния с полностью разорванными связями. Проблематичность такого допущения очевидна. [20]
Схемы эти делают понятной легкость сульфирования соединений, содержащих заместители первого рода, так как в этом случае прочность критического комплекса при вступлении заместителей в орто - и пара-положение должна быть выше. [21]
Однако легко представить себе возможность того, что первоначально сольватировавшийся атом с основными свойствами начнет вести себя при образовании критического комплекса как донор, теряя при этом свою способность образовывать координационные связи с растворителем. Это явление может перевесить увеличение сольватации за счет большой дипольной ассоциации. [22]
 |
Наблюдаемые и рассчитанные энергии активации для реакций в ацетоновом растворе. [23] |
Основной недостаток теории Огга - Поляни вытекает из их предположения, что достаточно рассмотреть только пересечение кривых в окрестности критического комплекса, не пытаясь выяснить зависимость энергии всей системы как непрерывной функции переменных T. Это допущение приводит к некоторым заключениям, противоречащим термодинамике. [24]
Схемы ли делают понятной легкость сульфирования соединении, содержащих заместители первого рода, так как в этом случае прочность критического комплекса при вступлении заместителей в орто - и пара-положение должна быть выше. [25]
 |
Влияние давления на скорость различных реакций. [26] |
Поскольку скорость большинства исследованных к настоящему времени реакций увеличивается с ростом давления, то можно заключить, что обычно объем критического комплекса меньше объема молекулы в нормальном, неактивированном состоянии. Другими словами, комплексы в переходном состоянии обычно более компактны, чем комплексы в основном состоянии. [27]
Для практического приложения ( П 29) необходимо, очевидно, обращаться к нашим весьма ненадежным сведениям о состоянии сольватации критического комплекса. Тем не менее вполне вероятно, что мы можем довольно правдоподобно оценить это состояние на основании нашего общего знания электронной теории. Так, в случае слегка полярных реагентов, которые рассматривал Белл ( см. выше), можно, повидимому, вполне законно думать, что критический комплекс также будет малополярным, а следовательно, степень его сольватации должна будет лишь незначительно меняться при протекании стадии, определяющей кинетику реакции. [28]
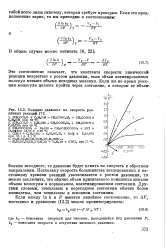 |
Влияние давления на скорость различных реакций. [29] |
Поскольку скорость большинства исследованных к настоящему времени реакций увеличивается с ростом давления, то можно заключить, что обычно объем критического комплекса меньше объема молекулы в нормальном, неактивированном состоянии. Другими словами, комплексы в переходном состоянии обычно более компактны, чем комплексы в основном состоянии. [30]
Страницы: 1 2 3 4
