Комплексант
Cтраница 2
 |
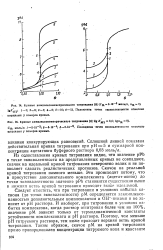
Диаграмма распределения различны се форм ЭДТА. i. [16] |
При комплексонометрическом титровании в раствор обычно добавляют дополнительный комплексант L для предотвращения осаждения определяемых ионов в виде гидроксидов или основных солей, а само титрование проводят в буферном растворе с большой буферной емкостью. Поэтому выделяющиеся по реакциям ком-плексообразования ионы Н30 практически не изменяют рН титруемого раствора. Если учесть, что титруемые катионы М также комплексуются посторонним комплексантом L и, кроме того, могут взаимодействовать с компонентами применяемого буферного раствора и ОН - - ионами, то становится очевидным, что при комплексонометрическом титровании на основное равновесие образования комплексо-ната металла всегда накладываются побочные конкурирующие равновесия с участием и титруемого иона и комплексона. Эти побочные равновесия препятствуют образованию комплексоната, снижают его выход и ослабляют его относительную устойчивость. Поэтому в реальных условиях анализа для оценки относительной устойчивости комплексоната металла и получения объективной информации о равновесной концентрации реагирующих веществ в процессе титрования необходимо использовать условные константы устойчивости комплексонатов металлов. [17]
Не меньшее значение имеет разделение ионов регулированием среды или введением комплексантов. В этом случае, как и всегда, выступает явление конкуренции между реагирующими ионами. Значение констант нестойкости позволяет ориентировочно предсказать воз-можноеть маскирования тех или других ионов в процессе их разделения. Следовательно, ион меди должен энергично связываться с тиосульфатом и будет им маскироваться; ионы кадмия будут маскироваться слабо, а ион цинка практически маскироваться не будет. [18]
Правильность выполненного расчета можно легко проверить соблюдением материального баланса по концентрации комплексанта ( лиганда), аналитическая концентрация которого, как правило, всегда известна. [19]
Так как Ks и / Ском специфичны для каждого металла и каждого комплексанта, обобщающие таблицы составить трудно. [20]
Рассмотренный выше материал по сорбции элементов ионитами из водно-органических растворов в присутствии неорганических и органических комплексантов показывает, что процессы сольватации и комплексообразования в фазе внешнего раствора могут быть движущей силой селективности и использованы для эффективных ионообменных разделений смесей ионов металлов. [21]
Подробно были изучены солюбилизация, экстракция и активация анионов карбоксилатов щелочных металлов различными комплексантами. [22]
Чему будет равна степень извлечения Fe ( III) при рН 2 в отсутствие посторонних комплексантов и при рН 7 в присутствии 0 01 моль / л ЭДТА. [23]
Сопоставление условных констант устойчивости комплексонатов меди и кальция показывает, что основное уравнение селективности в отсутствие посторонних комплексантов соблюдается при рН sj 7, однако при рН 5 значение Ссау еще достаточно высоко, чтобы можно было не считаться с ионами Са, не проводя их маскирование. [24]
Раствор содержит 0 9291 мг / мл ниобия ( V) и анионы SO - с комплексантом. [25]
Жидкая мембрана состоит из растворителя, не смешивающегося с водой, и реагента, выполняющего функцию экстрагента и комплексанта. Если такая жидкая мембрана разделяет два раствора, то ионная селективность достигается за счет преимущественной экстракции ионов в фазу мембраны, а также за счет разной подвижности ионов в пределах мембраны. Эйзенман [17] вывел уравнения для ряда жидких мембран, показав зависимость их селективности от степени диссоциации комплексов внутри мембраны, относительной подвижности ионов, ионообменных участков и комплексов. [26]
Следует отметить, что при титровании в условиях избытка катиона ( до точки эквивалентности) рМ определяется закомплексованностью дополнительным комплексантом и OHr-иснами и не зависит от рН раствора. И наоборот, при титровании в условиях избытка комплексона, когда раствор оттитрован более чем на 100 %, значение рМ зависит только от термодинамической константы устойчивости комплексоната и рН раствора. Поэтому, чем меньше рН титруемого раствора, тем ниже проходит верхняя ветвь кривой титрования. [28]
Из сопоставления значений растворимости осадка с общими концентрациями CNH и CNaCj видно, что сделанное допущение о равновесных концентрациях комплексантов вполне корректное. [29]
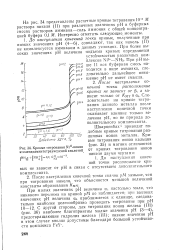 |
Кривые титрования Ы1 - ионов (. ис - 35 и ма отличаются этилендиаминтетрауксусной кислотой От кривых титрования ионов. [30] |
Страницы: 1 2 3 4