Остальные аминокислота
Cтраница 1
Остальные аминокислоты после их дезаминирования могут служить источником образования углеводов. [1]
 |
Навески аминокислот для приготовления 10 мл 0 01 Ж раствора. [2] |
Остальные аминокислоты при одновременном их присутствии в растворе полностью не разделяются. [3]
Все остальные аминокислоты после их дезаминирования могут служить источником образования углеводов. [4]
Большинство остальных аминокислот получает свою аминогруппу от одной из первичных аминокислот в результате трансаминирования. [6]
Концентрации остальных аминокислот были существенно снижены. Так, примерно в 3 раза снижено содержание тирозина, фенилаланина, изолейцина, треонина, гистидина, почти в 2 раза - содержание валина, лизина и лейцина. [7]
Что касается остальных аминокислот, то обозначение I сохраняется для активного изомера, найденного в белках, а обозначение d - для изомера, который является его зеркальным изображением по отношению к обоим центрам асимметрии. [8]
В отличие от остальных аминокислот молекулы глицина не имеют асимметрического атома углерода и поэтому в растворах оптически не активны. Однако в кристаллах глицина молекулы не плоские и могут существовать в виде двух зеркально связанных форм. [9]
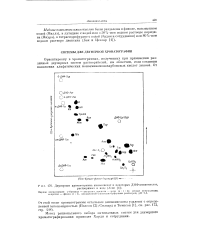 |
Двумерная хроматограмма аминокислот и некоторых ДНФ-аминокислот. [10] |
От этой оси хроматограммы остальные аминокислоты удалены с определенной закономерностью ( Полсон [2] Стьгоард н Томпсон [1], см. рис. 172, стр. [11]
Цис и Мет в его составе отсутствуют, остальные аминокислоты присутствуют в малых количествах. Рентгенограммы фиброина сходны с рентгенограммами - кератина, основная конформация - - форма. Шелк Bombyx mori образован полипептидом ( Гли - Ала), шелк Lyssax - полиаланином. О сократительных белках рассказано в гл. [13]
На колонке из окиси алюминия адсорбируется цистин, а все остальные аминокислоты удаляются водно-спиртовой смесью, подкисленной уксусной кислотой. Добавление формальдегида позволяет отделить серии и глицин на колонке из окиси алюминия, обработанной соляной кислотой. Удаляя из фильтрата формальдегид и доводя рН раствора до 5 5, адсорбируют аланин и пролин на колонке из флоридина. В растворе остаются лейцин, валин и метионин, которые разделяют на активированном угле. [14]
Аминокислота триптофан кодируется всего одним кодоном ( UGG), остальные аминокислоты, из которых состоят белки, - по крайней мере двумя, чаще четырьмя, а иногда и шестью колонами. Например, для лейцина существует шесть кодонов: UUA, UUG, CUU, CUC, CUA и CUG. Синонимичные кодоны используются различными организмами с разной частотой. Такая же ситуация наблюдается и для стоп-кодрнов. [15]
Страницы: 1 2 3 4 5

