Ионные мицелла
Cтраница 2
 |
Зависимость удельной электропроводности от концентрации ионного ПАВ.| Графическое определение мицеллярнои массы ПАВ по мутности. [16] |
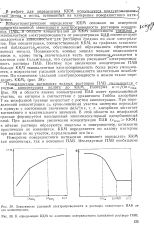
При этих кон центрациях начинают формироваться ионные мицеллы, окруженные диффузным слоем противоионов. Подвижность ионов при этом снижается и эквивалентная электропроводность уменьшается с увеличением концентрации резче, чем до критической концентрации мицеллообразования. В точке ККМ наблюдается также уменьшение скорости роста удельной электропроводности. [17]
Эта кривая приведена в подтверждение того, что ионные мицеллы начинают образовываться в точке В, и что они являются лучшими проводниками, чем простые ионы. Если не проанализировать этот вывод, то он может показаться неожиданным. [18]
Величина ш изменяется от 2 до 5 при образовании ионных мицелл в предмицеллярной области и от 10 до 100 - при образовании мицелл. [19]
Таким образом, чрезвычайно сильное замедление диффузии ионов и ионных мицелл тетраметилоктанбензолсульфоната в анионите ЭДЭ-10П не может быть вызвано лишь электрическим полем смолы, а связано скорее всего со стерическими ( пространственными) затруднениями, что хорошо видно на рассмотренном ранее примере поглощения ионов тетраметилоктанбензолсульфо-ната гелем анионита ЭДЭ-10П. Размеры этих ионов ограничивают возможность их диффузии в набухшей смоле проникновением только через элементарные ячейки размером не менее 9X9 А и при том лишь тогда, когда плоскости бензольных колец анионов ПАВ оказываются перпендикулярно ориентированными к плоскости просвета элементарной ячейки анионита. [20]
 |
Зависимость удельной электропроводности х раствора ионогенного ПАВ от его концентрации.| К определению ККМ по изменению поверхностного натяжения раствора ПАВ. [21] |
При концентрации, соответствующей ККМ, на графиках зависимостей наблюдается / излом, обусловленный образованием сферических ионных мицелл. Подвижность ионных мицелл меньше подвижности ионов и, кроме Toroj значительная часть противоионовунаходится в плотном слое Гельмгольца, что существенно уменьшает электропроводность раствора ПАВ. Поэтому при увеличении концентрации ПАВ больше ККМ эквивалентная электропроводность более резко уменьшается, а возрастание удельной электропроводности значительно ослабляется. [22]
Тем не менее нельзя не допустить и ту возможность, что, в результате адсорбции гегениойов, ионные мицеллы, находясь в углеводородных растворителях, способны переходить в состояние равновесия, аналогичное указанному выше. [23]
Лоттермозером s и другими авторами, указывают на любопытный факт: в растворах, настолько разбавленных, что ионные мицеллы в объемной фазе весьма немногочисленны или вовсе отсутствуют, конечное значение поверхностного натяжения достигается чрезвычайно медленно, иногда через несколько суток. [24]
 |
Схематическое изображение поперечного сечения мыльных мицелл. [25] |
Очевидно, что эти пластинчатые, сравнительно слабо заряженные мицеллы соответствуют нейтральным коллоидным частицам Мак-Бэна, отличаясь от меньших по размерам ионных мицелл, образующихся в более разбавленных растворах. [26]
 |
Константы скоростей реакций гидратированных электронов. [27] |
Константы скорости в воде для реакций с пиреном и бифенилом равны 1 1 1О и 5О 1О соответственно [33] Таким образом, наличие границы раздела не - ионных мицелл и воды, по-видимому, приводит к небольшому торможению реакции ( пирен), тогда как взаимодействие с бифени - лом почти не изменяется. Более высокая реакционная способность е - в случае бифени па может быть обусловлена его сопюбипизацией в областях более полярных, чем в случае пирена. Хотя дополнительной информации, свидетельствующей в пользу этого предположения нет, тем не менее можно думать, что в случае неионных мицелл отсутствуют барьеры, имеющие большой электрический заряд, подобные описанным для ионных мицелл. [28]
В предыдущей детальной работе были использованы, со ссылкой на еще более раннюю работу г 28 ], некоторые сульфофгалеиновые индикаторные красители для исследования поверхностного потен -, циала и рН поверхности ионных мицелл. [30]
Страницы: 1 2 3 4 5
