Ионные мицелла
Cтраница 4
 |
Схема строения сферической мицеллы ионо-генного ПАВ в воде ( - противоионы. [46] |
Мицеллы ионогенных ПАВ электрически заряжены вследствие диссоциации полярных групп. Благодаря сильному электростатическому притяжению значительное число противо-ионов ( до 80 % и более) связано с поверхностью мицеллы и составляет с ней единое целое с кинетической точки зрения, образуя штерновскую часть двойного электрического слоя. По расчетам Стигтера, толщина слоя Штерна на поверхности ионных мицелл - это величина порядка 0 215 - 0 4 нм, что примерно соответствует размеру полярных групп. [47]
Второй член в левой части (40.11) оказывает противоположное влияние по сравнению с первым, так что круглую форму можно объяснить явным преобладанием первого члена. Это свидетельствует о достаточно высоком значении ао на не занятой полярными группами поверхности. О третьем ( отрицательном) члене можно сказать, что для ионных мицелл он максимален по абсолютной величине в случае сферической формы, когда степень связывания про-тивоионов минимальна, а заряд мицеллы максимален. [48]
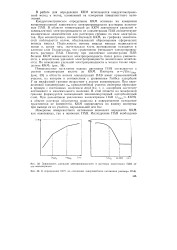 |
Зависимость удельной электропроводности и раствора ионогенного ПАВ от его концентрации.| К определению KKJV, по изменению поверхностного натяжения раствора ПАВ. [49] |
Кондуктометрическое определение ККМ основано на измерении концентрационной зависимости электропроводности растворов ионоген-ных ПАВ. В области концентраций до ККМ зависимости удельной и эквивалентной электропроводности от концентрации ПАВ соответствуют аналогичным зависимостям для растворов средних по силе электролитов. При концентрации, соответствующей ККМ, на графиках зависимостей наблюдается излом, обусловленный образованием сферических ионных мицелл. Гельмгольца, что существенно уменьшает электропроводность раствора ПАВ. Поэтому при увеличении концентрации ПАВ больше ККМ эквивалентная электропроводность более резко уменьшается, а возрастание удельной электропроводности значительно ослабляется. [50]
При дальнейшем увеличении концентрации ОМЭА электропроводность снова довольно резко надает и только после прохождения участка около 2 м М / л убывает более медленно. По-видимому, в области концентраций от 0 2 до 1 м М / л в водном растворе ОМЭА происходит процесс мицеллообразо-вания, в связи с чем и наблюдается излом кривой. По данным Мак-Бена и сотрудников [4], излом кривой эквивалентная электропроводность - концентрация для растворов коллоидных электролитов происходит при той концентрации, которая соответствует началу быстрого образования ионных мицелл. [51]
Константы скорости в воде для реакций с пиреном и бифенилом равны 1 1 1О и 5О 1О соответственно [33] Таким образом, наличие границы раздела не - ионных мицелл и воды, по-видимому, приводит к небольшому торможению реакции ( пирен), тогда как взаимодействие с бифени - лом почти не изменяется. Более высокая реакционная способность е - в случае бифени па может быть обусловлена его сопюбипизацией в областях более полярных, чем в случае пирена. Хотя дополнительной информации, свидетельствующей в пользу этого предположения нет, тем не менее можно думать, что в случае неионных мицелл отсутствуют барьеры, имеющие большой электрический заряд, подобные описанным для ионных мицелл. [52]
Характер полярной группы играет существенную роль при мицеллообразовании в водных и неводных средах. Ее влияние на ККМ отражает параметр а в уравнениях ( VI. Роль гидрофильных групп в водных растворах ПАВ заключается в том, чтобы удерживать образующиеся ассоциаты в воде и регулировать их размер. Сферическая форма ионных мицелл устанавливается, если энергия ассоциирования углеводородных цепей достаточно большая и превышает энергию электростатического отталкивания между ионными группами. Гидратация противоионов, окружающих мицеллу, способствует отталкиванию, а менее гидратированные ионы легче адсорбируются на поверхности мицелл. Наличие ионных концевых групп обеспечивает хорошую растворимость ПАВ в воде, поэтому для перехода ионогенных молекул в мицеллу требуется значительно больше энергии, чем для образования мицелл из неионогенных молекул. В связи с этим ККМ для ионогенных ПАВ значительно выше, чем для неионогенных, при одинаковой гидрофобности молекулы. Величина lg ККМ неионогенных ПАВ с полиоксиэтиленовой цепью растет с увеличением длины цепи по линейному закону. [53]
Характер полярной группы играет существенную роль при ми-целлообразовании в водных и неводных средах. Ее влияние на ККМ отражает параметр а в уравнениях ( VI. Роль гидрофильных групп в водных растворах ПАВ заключается в том, чтобы удерживать образующиеся агрегаты в воде и регулировать их размер. Сферическая форма ионных мицелл устанавливается, если энергия агрегирования углеводородных цепей достаточна, чтобы превзойти электростатическое отталкивание между ионными группами. Гидратация противоионов способствует отталкиванию, а менее гидратированные ионы легче адсорбируются на поверхности мицелл. Наличие ионных концевых групп обеспечивает хорошую растворимость ПАВ в воде, поэтому для перехода ионогенных молекул в мицеллу требуется значительно больше энергии, чем для неионогенных молекул. В связи с этим ККМ для ионогенных ПАВ значительно выше, чем для неноногенных, при одинаковой гндрофобности молекулы. Величина lg ККМ неионогенных ПАВ с полиоксиэтиле-новой цепью растет с увеличением длины цепи по линейному закону. [54]
Турбидиметрический метод определения внутримицелляр-ной растворимости рекомендуется в случае солюбилизации полярных органических веществ, например жирных спиртов. В этом случае, как уже отмечалось, солюбилизация приводит к образованию смешанных мицелл: полярные молекулы добавки, внедряясь в м целлы, располагаются в них аналогично молекулам мыла. Наличие неионизированных полярных групп в гидрофильной внешней части мицелл понижает плотность их поверхностного электрического заряда ( и, следовательно, величину электростатической составляющей энергии мицеллообразования), что способствует укрупнению мицелл. Поскольку неионизированные полярные группы менее гидрофильны, чем заряженные, их внедрение в ионные мицеллы ослабляет гидрофильные свойства последних, что также способствует укрупнению мицеллярных агрегатов. Другими словами, полярные органические добавки гидрофо-бизируют мицеллы, снижают их устойчивость. [55]
Мыль ные растворы обладают такой же эквивалентной проводимостью, как растворы простых солей. Этот факт может показаться неожиданным, если учесть известную мицеллярную структуру мыльных растворов. Это наблюдение натолкнуло Макбэйна ( см. ссылку 161) еще в 1913 году на мысль определить понятие коллоидного электролита ионной мицеллы. Согласно его теории, коллоидные электролиты являются растворами, которые содержат крупноразмерные ионы или ионные мицеллы, представляющие собой агрегаты из многих отдельных ионов. Так, например, если мицелла состоит из 50 ионов олеата натрия, то это обозначает, что она содержит 50 отрицательных зарядов. Следовательно, если речь идет Об ионном заряде, то объединение в мицеллы ни в коем случае не - приводит к уменьшению электропроводности раствора. [56]
С другой стороны, многие числа мицегшярной агрегации согласуются с образованием сферических мицелл, радиус которых примерно равен длине мономера. Например, додецилсульфат натрия в воде имеет величину / Vm, равную 5719, что характерно для сферической мицеллы. Качественн Ое рассмотрение относительного положения максимума In К максимума ( n q / q и максимума кривой распределения по размерам показывает, что для таких систем 1пК имеет максимум при q более низком, чем это требуется для сферических мицелл с радиусом порядка длины цепи мономера. Несколько лет назад Стиг - тер и Овербек [35] исследовали такие изменения, используя сферическую модель ионных мицелл Макдовел и Краус [36] нашли, что для некоторых систем ионных ПАВ с очень длинными цепями, например для и - октадешптрибутиламмонийбромата, эквивалентная электропроводность дри критической концентрации резко повышается затем проходит через максимум и понижается. Повышение электропроводности - указывает на присутствие весьма малых мицелл. Стиг - тер [37] проанализировал эти данные и показал, что весьма малые мицеллы должны быть полидисперсны. В системах такого рода узкому распределению мицепп среднего размера, возможно, должен предшествовать интервал концентраций. [57]
 |
Зависимость удельной электропроводности раствора ионогенного ПАВ от его концентрации.| Графическое определение мицеллярной массы ПАВ по мутности раствора. [58] |
Кондуктометрический метод применяется для определения ККМ ионогенных ПАВ. Зависимость эквивалентной электропроводности от концентрации ПАВ отличается от аналогичной зависимости для растворов простых электролитов. В области до KKMi водные растворы ПАВ обнаруживают отклонение от уравнения Онзагера ( линейное уменьшение эквивалентной электропроводности в зависимости от с - ) в той же степени, которая характерна для средних по силе электролитов. Однако уже при малых концентрациях ( 10 - 3 моль / л) на кривой концентрационной зависимости эквивалентной электропроводности наблюдается излом. При этих концентрациях начинают формироваться ионные мицеллы, окруженные диффузным слоем про-тивоионов. Подвижность ионов при этом снижается и эквивалентная электропроводность уменьшается с увеличением концентрации резче, чем до критической концентрации мицеллообразования. В точке ККМ наблюдается также уменьшение наклона подобной зависимости для удельной электропроводности. [59]
Согласно (15.11), величины Ка и Кс отличаются друг от друга множителем, в который входят коэффициенты активности. В соответствии со сделанным выше замечанием к формуле (15.7) коэффициенты активности мономеров fu можно трактовать более широко как относящиеся к свободной ( не-мицеллярной) форме ионов и молекул в растворе, включающей образование мелких ассоцнатов, если они возникают. В случае разбавленных растворов, какими являются обычно мицелляр-ные системы в районе ККМ, коэффициенты активности свободных ионов близки к единице, но, поскольку они все же меньше единицы, то, будучи возведенными в большие степени п, МОГУТ оказаться весьма малыми величинами. Что касается коэффициента активности мицелл f, то он уже в районе КММ может оказаться малым из-за большого заряда мицеллы. Поэтому, по крайней мере, для ионных мицелл, априори трудно полагать fn / м 1 для оправдания условия Кс К const в записи (15.10), которая обычно используется на практике. [60]
Страницы: 1 2 3 4 5