Ионные мицелла
Cтраница 3
Влияние образования ионных мицелл внутри растворов этих солей на их поверхностное натяжение представляет большой интерес. Хотя ионные мицеллы значительно более растворимы и, вероятно-гораздо менее поверхностно-активны чем отдельные ионы, их присутствие внутри раствора обусловливает гораздо более быстрое понижение поверхностного натяжения до минимума. Причина этого явления неясна, но возможно, что накопление неассоциированных ионов на поверхности облегчается их электростатическим взаимодействием с крупными зарядами мицелл. [31]
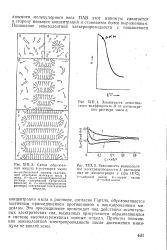
При концентрации, соответствующей ККМ, на графиках зависимостей наблюдается / излом, обусловленный образованием сферических ионных мицелл. Подвижность ионных мицелл меньше подвижности ионов и, кроме Toroj значительная часть противоионовунаходится в плотном слое Гельмгольца, что существенно уменьшает электропроводность раствора ПАВ. Поэтому при увеличении концентрации ПАВ больше ККМ эквивалентная электропроводность более резко уменьшается, а возрастание удельной электропроводности значительно ослабляется. [32]
Экспериментально было показано, что совмещение сульфонатной присадки с алкилфенолятной ( внии нп-370 алкилфенолятная присадка формальдегид-ной конденсации) резко повышало диссоциацию последней в масле и обеспечивало высокую электропроводность масла с этими присадками, и, следовательно, высокий моющий эффект. Было также показано, что именно ионы ( или ионные мицеллы) алкилфенолятной присадки сорбируются на поверхности сажи и окиси железа и обеспечивают электростатический эффект. [33]
Один - сферическая ионная мицелла, состоящая не более чем из 10 одинаковых ионов, сохраняющих свои заряды - образуется в разбавленном растворе немного ниже ККМ; другой - мицелла с малым зарядом или совсем не имеющая его - образуется при ККМ. Таким образом, согласно Мак-Бэну, раствор содержит как высоко проводящие ионные мицеллы, так и практически не проводящие тока пластинчатые мицеллы. Сочетание этих двух видов мицелл объясняет форму кривой электропроводности. [34]
Гартли, обусловливается частичным присоединением противоионов к ионизированным мицеллам. Это присоединение происходит под действием значительных электрических сил, вызванных присутствием образовавшихся в системе высокозаряженных ионных мицелл. Причины повышения эквивалентной электропроводности после достижения минимума не вполне ясны. [36]
Это не было бы, как это иногда предполагается, несовместимым со значительным понижением поверхностного натяжения: возможно, что неоднородная поверхностная фаза имеет толщину, превышающую размеры одной молекулы, причем молекулы растворенного вещества ориентированы в ее наружной части таким образом, что их гидрофобные группы покрывают значительную часть поверхности; непосредственно под крайними молекулами может приходиться больше молекул воды на каждую молекулу растворенного вещ. Не вполне ясно, почему гидратация растворенного вещества в поверхностной фазе сильнее, чем внутри, но это может быть обусловлено образованием ионных мицелл в объемной фазе, которые могут слабее гидратироваться, чем отдельные ионы, образующие адсорбционный слой. Можно ожидать некоторого понижения поверхностного натяжения при выходе на поверхность любых молекул, содержащих гидрофобные части, так как п ле их сил притяжения слабее поля чистой вод ч Это может происходить и в поверхностной фаз % содержащей меньше молекул растворенного вещества, чем объемная фаза, хотя нельзя ожидать большого понижения поверхностного натяжения иначе, как при известном накоплении более гидрофобного растворенного ещества во внешнем слое поне хностной фазы. Пожалуй, вес ма показательно, что для солей с парафиновой цепью минимум поверхностного натяжения наблюдается при концентрациях того же порядка, что и ко центрации, при которых мицеллы образуются в больших количествах внутри раствора, и что точное значение концентрации зависит от присутствия геболь-ших посторонних примесей в воде. [37]
Особенно хороша модель сферического конденсатора в применении к цвиттерионным ПАВ. В их молекулах противоположные заряды удалены друг от друга, а в мицеллах образуется четкий сферический конденсатор с энергией, близкой к таковой для ионных мицелл. [38]
Сделан обзор характерных особенностей локального микроокружения в различных областях водных мицеллярных систем, и представлены некоторые новые результаты. Эти различные области включают: углеводородное ядро; метиленовые группы, близкие к полярным головкам; поверхность раздела мицелла - вода вместе с наиболее глубокой частью двойного электрического слоя ( слоя Штерна) для ионных мицелл, внешнюю часть диффузных двойных слоев и оболочку, образованную полиоксиэтиленовыми группами в некоторых неионогенных ПАВ. Рассматриваются различные факторы влияющие на эффективную полярность раздела мицелла - вода, и представлены некоторые новые результаты, приводящие к мысли, что близость углеводородного ядра и частичное диэлектрическое насыщение у поверхности раздела являются факторами, способствующими ближним взаимодействиям. Некоторые новые результаты по константам диссоциации индикаторных красителей, растворенных в мицеллах неионогенных и цвиттер-ионных ПАВ, указывают на существенную роль локального микроокружения. Обсуждаются особенности микроокружения, в котором находятся молекулы солюбилизованного вещества. Представлены некоторые результаты, указывающие на то, что окружение солюбилизованных бензола и нафталина весьма полярно. Эти наблюдения объяснены исходя из того, что солюбилизация происходит главным образом на поверхности раздела. Из термодинамических соображений следует, что этот эффект может быть приписан предполагаемой слабой поверхностной активности бензола в системах углеводород - вода, который становится важным для мицелл из-за чрезвычайно высокого отношения величин площади поверхности к объему. Кратко суммируются некоторые общие следствия из этих результатов для процессов, протекающих в коллоидных системах, на поверхности раздела и в мембранах. [39]
Некоторые из методов, описанных ниже, были разработаны Бьеррумом [6] и Кройцером [36] для исследования равновесий в газовой фазе. При исследовании ассоциации в растворах форма В обычно является незаряженной органической молекулой, которая способна к образованию межмолекулярной водородной связи, но настоящая обработка результатов в равной мере применима, например, к образованию ионных мицелл или к димеризации свободных радикалов. При других условиях центральная группа может сама по себе диссоциировать. Например, в органических растворителях карбоновые кислоты можно рассматривать как недиссоциированную группу В, но в водном растворе они заметно диссоциируют как протонный комплекс HjA. Более сложные полиядерные формы В Ар ( р0), которые содержат как центральную группу, так и лиганд, рассматриваются в гл. Смешанные комплексы ВдА - рЩ, которые являются полиядерными по отношению к В и содержат два типа лигандов, обсуждаются в гл. [40]
Во многих случаях, в особенности при эмульгировании, важно подуть как можно более низкое межфазное натяжение между водным раствором и маслом. Как указывает Гартли2, натриевые и другие одновалентные соли с парафиновой цепью ( нипример, C16H33OSO3Na) понижают поверхно: тное натяжение между чистым углеводородным маслом и водой не более, как на 1 - 2 дин см. Это приписываемся легкости образования ионных мицелл этих солей в растворе. Эти мицеллы представляют собой агрегаты ионов, в которых гидрофильные концы обращены наружу, и углеводородные цепи скрыты внутри, так что они обладают большой раств ри-мостью в вэде - гораздо большей, чем отдельные ионы. Поскольку эти мицеллы образуются при низких концентрациях, концентрация отдельных ионов в растворе не может быть достаточной для большого понижения пэверхностного натяжения. [41]
Влияние заряда поверхности на адсорбцию может быть весьма сильным. Если мицеллы состоят из агрегированных анионов последовательно, имеют отрицательный заряд, то равновесие индикатора в растворе смещается таким образом, чтобы присутствовало большее количество положительно заряженного индикатора и меньшее количество отрицательно заряженного. Ионные мицеллы, состоящие из катионов, смещают равновесие в обратную сторону. [42]
Тенденция поверхностно-активного вещества к выделению из системы при превышении критической концентрации проявляется в том, что оно концентрируется на поверхностях раздела или образует в системе агрегаты молекул. Точное строение таких агрегатов еще не установлено, однако существуют концепции, позволяющие до некоторой степени объяснить практический эффект, вызываемый их образованием. Ионные мицеллы рассматривают как сферы, в которых ионные головки направлены наружу, в случае водных систем, а лиофильные цепи образуют ядро. В неводных системах полярные головки направлены внутрь мицелл, а углеводородные цепи - наружу. Выделение поверхностно-активного вещества из системы под действием растворителя определяется размерами и полярностью двух пр. От этих факторов зависит природа и эффективность поверхностно-активных веществ. [43]
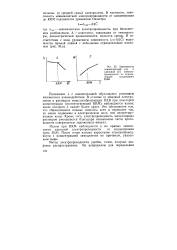 |
Зависимость эквивалентной ( а и удельной ( б электропроводности от концентрации коллоидного ОАВ. [44] |
Понижение К с концентрацией обусловлено усилением межионного взаимодействия. В отличие от обычных электролитов в растворах мицеллообразующих ПАВ при некоторой концентрации ( соответствующей ККМ) наблюдается излом, после которого К падает более круто. Это объясняется тем, что образующиеся ионные мицеллы хотя и переносят ток, но менее подвижны в электрическом поле, чем неагрегированные ионы. Кроме того, электропроводность мицеллярных растворов уменьшается благодаря связыванию части проти-воионов поверхностью заряженных мицелл. [45]
Страницы: 1 2 3 4 5