Мембранные белок
Cтраница 3
В работе [188] сделана попытка исследовать поведение мембранных белков с помощью радикала BVII, ковалентно связанного с белками мембран саркоплазматического ретикулума. Этот может быть связано с тем, что спиновая метка достаточно далеко отстоит от поверхности белка и поэтому прежде всего отражает конформационные изменения в ее липидном окружении. По-видимому, для более полной информации о белке необходимо использовать радикалы, более жестко связанные с белками мембран. [31]
 |
Модель Синджера - с она. [32] |
В середине 60 - х годов химия мембранных белков только зарождалась и делались первые попытки найти подходы к разработке методов их выделения и характеристики. Многие мембрано-связанные белки обладают ферментативной активностью. В ряде случаев экстракция липидов из мембраны приводила к полной утрате или к значительному снижению ферментативной активности. [33]
 |
Жвдкостно-мозаичная модель структуры мембран, предложенная Сингером и Николсоном. [34] |
Далее, из жидкостно-мозаичной модели следует, что мембранные белки мо. [35]
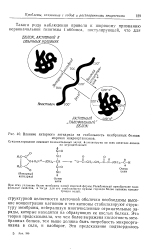
Наиболее широко применяемый в настоящее время метод солюбнлнзацин мембранных белков - это разрушение липндкого бислоя детергентами. Чтобы в максимальной степени сохранить нативную кинформацию выделяемого белка, необходимо использовать для солюбнлизации неденатурирующие детергенты. К ним, напри мер, относятся соли желчных кислот или их производные. Для солюбнлизации и очистки мембранных белков используются также такие неионные детергенты, как тритон, нонидет, эмульфоген, сктилглюкозид и др. Интегральные белки, солюби-лизированные солями желчных кислот или неионными детергентами, как правило, сохраняют свою биологическую активность. [36]
Основные работы связаны с изучением структуры и функции мембранных белков методом кристаллографии. [37]
 |
Влияние янтарного ангидрида на стабильность мембранных белков морских микроорганизмов. [38] |
Эта теория предсказывала, что чем более выражена кислотность мембранных белков, тем выше должна быть потребность микроорганизма в соли, и наоборот. [39]
 |
Трансмембранная передача информации с участием аденилатциклазы ( АС и ГТФ-связывающих белков. [40] |
Приведенные примеры указывают на важное биологическое значение олигомерных ассоциатов мембранных белков, состоящее в том, что при изменении физико-химических свойств мембраны соответственно изменяется и характер взаимодействия мембранных структур. Таким образом формируются обратные связи для приспособления обмена веществ к потребностям организма. [41]
Жидкомозаичная модель Синджера и Николсона [3] различает два типа мембранных белков: периферические и интегральные. Периферические белки удерживаются на поверхности мембраны в основном ионными взаимодействиями и относительно легко солюбилизируются, например, путем увеличения ионной силы. Интегральные белки погружены в липидную фазу и не могут быть высвобождены из мембраны без хотя бы частичного ее разрушения. Они нерастворимы в воде, гидрофобны и липофильны. Эта характеристика двух классов мембранных белков предполагает, что они асимметрично распределены в клеточной мембране: периферические белки находятся только по одну сторону бислоя, тогда как интегральные проникают в нее - чаще только в один монослой; если же они пронизывают весь бислой, то тогда они функционально асимметричны. [42]
Имеются сведения, что из фосфолииида остатки Сахаров передаются в мембранные белки, которые и являются местом синтеза полисахаридных цепей. После завершения синтеза молекул матричных полисахаридов они, по-видимому, освобождаются от белка. [43]
Учитывая неопределенность количественных оценок мембранных липидов и недостаток наших знаний относительно мембранных белков, легко понять, почему количественно охарактеризовать структуру мембран и механизм их действия мы пока не в состоянии. В настоящее время оказывается возможным лишь изучать свойства простых модельных мембран, с тем чтобы вывести по аналогии те или иные заключения, применимые к природным мембранам. [44]
 |
Гидрофобности аминокислотных остатков. [45] |
Страницы: 1 2 3 4 5