Окисление - линолеат
Cтраница 1
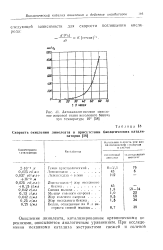 |
Автокаталитическое окисление жировой ткани несоленого бекона при температуре 10. [1] |
Окисление линолеата, катализированное органическими перекисями, описывается аналогичным уравнением. [2]
Кинетика окисления коллоидального линолеата описывается соотношением, приведенным на стр. [3]
При окислении линолеатов и линоленатов происходит изомеризация несопряженных двойных связей в сопряженные. В линолена-тах возможно образование группы гидроперекиси и сопряженных диенов или двух групп гидроперекиси и сопряженных триенов. [4]
Основными катализаторами окисления линолеата, очевидно, являются миоглобин и гемоглобин, так как белковые экстракты свиной ткани промотируют цепную реакцию окисления. Коагуляция белков значительно уменьшает каталитическую активность гемовых соединений. [5]
Очевидно, в результате окисления линолеатов несопряженные связи превращаются в сопряженные и у углеродного атома, смежного с этой системой, образуется гидроперекись. Возможно, что когда гидроперекиси разлагаются, то катализируется полимеризация сопряженной системы одной молекулы с непредельными связями другой молекулы с образованием прямой связи С-С между двумя молекулами. [6]
Очевидно, в результате окисления линолеатов несопряженные связи превращаются в сопряженные и у углеродного атома, смежного с этой системой, образуется гидроперекись. Возможно, что когда гидроперекиси разлагаются, то катализируется полимеризация сопряженной системы одной молекулы с непредельными связями другой молекулы с образованием прямой связи С - С между двумя молекулами. [7]
Было показано [58], что окисление линолеата катализируется экстрактами мышечной и жировой тканей свиней, причем нагревание уменьшает каталитический эффект, но не уничтожает его. [8]
Аскорбиновая кислота действует синергетически с малыми количествами а-токоферола, предохраняя ускорение окисления линолеата цнтохромом с; возможно, что аскорбинат восстанавливает смесь окисленных продуктов токоферола. [9]
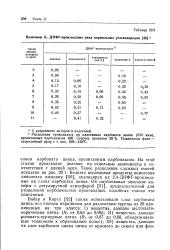 |
Величины RJ ДНФГ-производных ряда нормальных углеводородов а. [10] |
На этой стадии происходит деление на отдельные компоненты в соответствии с длиной цепи. Такое разделение сложных смесей показано на рис. 20.1. Бедингз исследовал продукты окисления линолеата аммония [50], анализируя их 2 4 - ДНФГ-производ-ные на слоях карбоната цинка. [11]
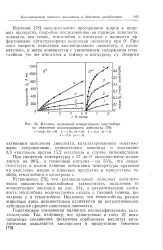 |
Влияние начальной концентрации миоглобинл. [12] |
Установлено [79], что коллоидальный линолеат каталитически окисляется миоглобином ( зависимость окисления от концентрации показана на рис. 33), а каталитическая активность миоглобина количественно сходна с таковой гемина, цитохрома с и гемоглобина. Показано, что гемоглобины разных животных лишь незначительно отличаются по каталитическому действию на процесс окисления линолеата. [13]
Как видно из рис. 34, примерно через 10 часов скорость реакции в присутствии гемина уменьшается, что объясняется разрушением катализатора. Установлено, что в процессе разрушения перекиси линолеата происходит образование карбонильных соединений; одновременно разрушается гематин. Продукты катализированного гемоглобином окисления линолеата спектрально характеризуются величиной поглощения при 232 и 278 ммк. [14]
Страницы: 1