Молекулярная орби-таль
Cтраница 1
 |
Молекулярные орбитали бензола и тритила. Стрелками показаны наиболее вероятные электронные переходы. А - разрыхляющие. Б - несвязывающие. В - связывающие орбитали. [1] |
Молекулярные орби-тали в свою очередь распадаются на равное число связывающих и разрыхляющих орбиталей, энергии которых равны по величине, но имеют противоположный знак, а оставшиеся орбитали ( если углеводород нечетный) - несвязывающие и имеют нулевую энергию. [2]
 |
Энергетические уровни молекулярных орбиталей, показанных на 12 - 7. Среди молекулярных орбиталей, образованных атомными s - и р-орбиталями, связывающие устойчивее. [3] |
Молекулярные орби-тали кх и лу устойчивее ст2 - орбитали, поскольку они позволяют электронам оставаться дальше от заполненной а5 - орбитали. [4]
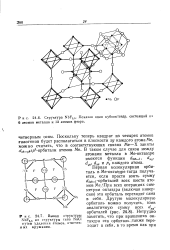 |
Структура NbF2. 5. Показан один кубооктаэдр, состоящий из атомов металла и 12 атомов фтора. [5] |
Первая молекулярная орби-таль в Ме-октаэдре тогда получается, если просто взять сумму зг2 - i-орбиталей всех шести атомов Ме. [6]
 |
Вид некоторых орбита-лей, направленных вдоль межъядерной оси, показывающей, как определяются а -, я - и б. - твдш ор-биталей. [7] |
Молекулярную орби-таль этого типа называют cr - МО. Она может образоваться только при перекрывании ( или -) двух атомных орбиталей, которые также обладают тем же свойством относительно рассматриваемой оси. Такие атомные орбитали можно обозначать символом а, В приведенном выше наборе таким свойством обладают только атомные s - и р2 - орбитали. [8]
Связывающая молекулярная орби-таль имеет более низкую энергию, чем атомная ls - орбиталь водорода, поэтому она называется связывающей орбиталью; она более стабильна, чем две отдельные атомные орбитали водорода. [9]
 |
Строение молекулы воды.| Модель расчета энергии. [10] |
Система молекулярных орби-талей в молекуле воды изображена на рис. 2.1, б, где восемь внешних электронов движутся по четырем эллиптическим орбиталям. Оси двух из них совпадают с направлениями валентных связей Н - О, а оси двух других расположены в перпендикулярной плоскости и пересекают ядро атома кислорода. [11]
 |
Строение молекулы воды.| Модель расчета энергии. [12] |
Система молекулярных орби-талей в молекуле воды изображена на рис. 2.1, б, где восемь внешних электронов движутся по четырем эллиптическим орбиталям. Оси двух из них совпадают с направлениями валентных связей Н - О, а оси двух других расположены в перпендикулярной плоскости и пересекают ядро атома кислорода. Согласно электронной структуре молекулы воды, в ней должны быть четыре пространствен. [13]
 |
Электронная плотность на низшей ( я и высшей ( б орбиталях. [14] |
Если метод молекулярных орби-талей ( МО), использованный при рассмотрении указанной выше структуры этилена ( см. рис. 4), применить к бутадиену, то можно получить две заполненные молекулярные орбитали. [15]
Страницы: 1 2 3 4 5