Молекулярная орби-таль
Cтраница 5
Наглядное изображение электронного распределения в кова-лентной молекуле Н2, полученное с помощью ЭВМ в рамках теории молекулярных орби-талей по методу ЛКАО. [61]
 |
Значения энергии ВЗМО и НСМО ряда алкилфенолов. [62] |
При этом предполагается осуществление связи ароматического соединения с катализатором за счет частичного перехода л-элек-трона соединения с верхней заполненной молекулярной орби-тали ( ВЗМО) на вакантную орбиталь металла катализатора и обратного перехода электрона металла на нижнюю свободную молекулярную орбиталь ( НСМО) реагирующей молекулы. Первый вид взаимодействия обычно называют донорно-акцептор-ным, а второй - дативным. [63]
Как правило, достаточно иметь такую информацию для высшей занятой молекулярной орбитали ( ВЗМО) и низшей свободной молекулярной орби-тали ( НСМО) реагирующих веществ. [65]
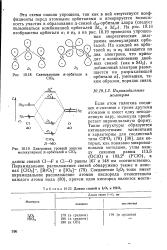 |
Диаграмма уровней энергии новыми методами, углы межмолекулярных я-орбиталей в СЮ2. ду связями равны 1 / 13 5.| Длины связей в ЬО5 и НЮ3. [66] |
На рис. 10.18 изображены орбитали я и пг, а на рис. 10.19 приведена упрощенная энергетическая диаг-рамма молекулярных орби-талей. [67]
Страницы: 1 2 3 4 5
