Молекулярная орби-таль
Cтраница 4
Однако сторонники теории МО легко парируют это замечание, поскольку рассмотренные выше молекулярные орби-тали, делокализованные по ядерному остову молекулы, нетрудно преобразовать в набор локализованных орбиталей, относящихся к различным участкам молекулы. Таким образом, этот недостаток теории МО преодолевается путем математических преобразований. [46]
Объяснение этому факту дает другой метод описания химической связи - метод молекулярных орби-талей. [47]
 |
Перекрывание атомных орбиталей в молекуле диборана. [48] |
Пунктиром на этой схеме показаны трехцентросые связи: здесь общая пара электронов занимает молекулярную орби-таль, охватывающую три атома-мости-ковый атом водорода и оба атома бора. [49]
Для ионов с конфигурацией d3 дополнительное сверхтонкое взаимодействие должно быть малым, так как молекулярные орби-тали симметрии t2g, на которых находятся неспаренные электроны, не содержат s - орбиталей атомов лигандов, которые дают основной вклад в константы дополнительного сверхтонкого расщепления. [50]
Как видно, в отличие от рассматривавшегося выше метода валентных связей, квантово-химический метод молекулярных орби-талей дает ясное и четкое представление о физической сущности явления ароматичности. Взамен весьма нечетких использовавшихся ранее химических критериев ароматичности из него вытекает следующее определение: ароматическими являются такие ненасыщенные циклические соединения, у которых все атомы цикла принимают участие в образовании единой сопряженной системы, а я-электроны этой системы образуют замкнутую электронную оболочку, полностью заполняя связывающие молекулярные орбитали. [51]
В разделе (15.5) мы рассмотрим интерпретацию региоселектив-ности реакций & г с точки зрения теории молекулярных орби-талей. Однако предварительно следует подчеркнуть, что ориентация нуклеофильного замещения чрезвычайно чувствительна к пространственным эффектам. [52]
Наиболее обобщенной и перспективной теорией, объясняющей строение и свойства комплексов, является теория молекулярных орби-талей. Она рассматривает комплексообразователь и лиганды как единое целое - комплекс. [53]
Как видно, в отличие от рассматривавшегося выше метода валентных связей, квантово-химический метод молекулярных орби-талей дает ясное и четкое представление о физической сущности явления ароматичности. Взамен весьма нечетких использовавшихся ранее химических критериев ароматичности из него вытекает следующее определение: ароматическими являются такие ненасыщенные циклические соединения, у которых все атомы цикла принимают участие в образовании единой сопряженной системы, а я-электроны этой системы образуют замкнутую электронную оболочку, полностью заполняя связывающие молекулярные орбитали. [54]
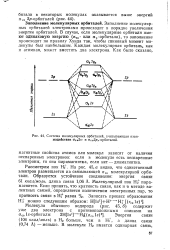 |
Система молекулярных орбиталей, учитывающая взаимодействие 0св2 - и 0Св2ра. - орбиталей. [55] |
На рис. 45, а видно, что единственный электрон размещается на связывающей асв молекулярной орби-тали. Образуется устойчивое соединение: энергия связи 61 ккал / моль, длина связи 1 06 А. [56]
Только теперь конфигурациям метода МО, в котором слейтеровские определители были построены из функций молекулярных орби-талей ij) s или я) А, соответствуют комбинации метода ВС с определителями, сформированными из атомных функций фА или фв. Это означает, что возможные антисимметричные комбинации из пространственных и спиновых функций - здесь их тоже шесть - соответствуют состояния с электронами, локализованными на определенных атомах. Таким образом, в методе ВС в некоторой степени будут заселены и атомные орбитали, тогда как в трактовке МО речь идет о молекулярных орбиталях, распространяющихся на всю молекулу и обнаруживающих определенную пространственную симметрию. [57]
Перенос заряда в большинстве случаев происходит с наиболее высокой занятой молекулярной ор-битали донора на наиболее низкую свободную молекулярную орби-таль акцептора, причем переход одного из пары внешних электронов донора, занимающих молекулярную орбиталь грд, на незанятую молекулярную орбиталь Я ЗА осуществляется без изменения спина электрона. Второй электрон на я зд остается спаренным с электроном, находящимся теперь на i) A. В результате образуется ковалент-ная связь. Коэффициенты а и b в уравнении (1.1) характеризуют долю структуры без связи и структуры с переносом заряда в основном состоянии комплекса. [58]
Предполагается, что первых четыре возбужденных состояния молекулы водорода связаны с нахождением одного электрона в молекулярной орби-тали, основанной на 2s - или 2р - орбитали атома водорода. [59]
Связывающие электроны в молекуле движутся в поле всех ядер молекулы, следовательно, находятся на молекулярных орби-талях. Однако, когда у атома имеются электроны на наполовину заполненных орбиталях, дополнительные незанятые орбитали или когда связывающих электронов слишком мало или слишком много, необходимо обратиться к методу молекулярных орбиталей. Появляются новые понятия: разрыхляющие орбитали, несвязывающие орбитали, кратные связи, триплетные состояния, промотирование, гибридизация и дело-кализация. [60]
Страницы: 1 2 3 4 5