Поверхность - оксид - алюминий
Cтраница 1
Поверхность оксида алюминия, как уже отмечалось, имеет основные центры, обеспечивающие преимущественную адсорбцию кислых соединений, содержащихся в нефтепродуктах: кислот, фенолов, пирролов. При обработке его кислотой получают адсорбент, обладающий кислыми свойствами. Обе формы оксида алюминия, основная и кислая, обладают склонностью к ионному обмену и проявляют заметную каталитическую активность, приводящую к разложению некоторых веществ при адсорбции. Для жидкостно-адеорбционной хроматографии наиболее пригоден нейтральный оксид алюминия, который получают мягкой нейтрализацией кислого или основного материала. Такой оксид алюминия не проявляет заметных каталитических и ионообменных свойств. [1]
Поверхность оксида алюминия, как уже отмечалось, имеет основные центры, обеспечивающие преимущественную адсорбцию кислых соединений, содержащихся в нефтепродуктах: кислот, фенолов, пирролов. При обработке его кислотой получают адсорбент, обладающий кислыми свойствами. Обе формы оксида алюминия, основная и кислая, обладают склонностью к ионному обмену и проявляют заметную каталитическую активность, приводящую к разложению некоторых веществ при адсорбции. Для жидкостно-адсорбционной хроматографии наиболее пригоден нейтральный оксид алюминия, который получают мягкой нейтрализацией кислого или основного материала. Такой оксид алюминия не проявляет заметных каталитических и ионообменных свойств. [2]
На поверхности оксида алюминия гидроксилы ведут себя как бренстедовские кислотные центры, а свободные соседние атомы алюминия вследствие дефицита электронов оказываются кислотными центрами льюисовского типа. Пери [1-4] обратил внимание на то, что донорами электронов на поверхности оксида алюминия могут быть двойные и тройные кислородные дефекты кристаллической решетки. [3]
Заряд поверхности оксида алюминия, как и кварца, определяется соотношением положительно и отрицательно заряженных активных центров, которое, в свою очередь, зависит от концентрации ионов Н и ОН - в растворе. [5]
 |
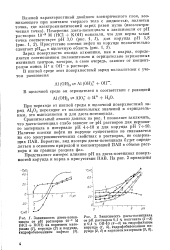
Соотношение вода. хлор в зоне катализа и содержание хлора в катализаторе по патентным данным. [6] |
Состав поверхности оксида алюминия находится в динамическом равновесии с составом газовой фазы над ней. Поэтому, изменяя соотношение воды и хлора в газовой фазе, можно регулировать в катализаторе содержание хлора, абсолютное количество которого будет зависеть также и от температуры, и от свойств самого оксида алюминия. Указания на такой метод регулирования содержания хлора в катализаторах имеются в патентной литературе. [7]
Заряд поверхности оксида алюминия, как будет показано ниже в разд. [9]
 |
Влияние среды на активность. [10] |
Хлорирование поверхности оксида алюминия, сопровождающееся выделением хлороводорода и диоксида углерода, усиливает кислотность апротонного и протонного типа. [11]
Гидратация активных центров поверхности оксида алюминия и ионизация поверхностных гидроксилов с отщеплением протона приводят к появлению у поверхности оксида алюминия электрического заряда, величина которого существенно зависит от рН, так как Н - и ОН - - ионы являются потенциалопределяющими ионами поверхности. Знак заряда поверхности изменяется в границах рН 7 - 9, и потому оксид алюминия является ионообменни-ком амфотерной природы. [12]
Конечным продуктом реакции на поверхности оксида алюминия является галлоизит. [13]
 |
Влияние влажности адсорбированной воды облег. [14] |
Ионы ОН, находящиеся на поверхности оксида алюминия, как и гидроксилы коллоидного осадка гидроксида алюминия, способны к обмену с анионами и катионами. Так, способность к адсорбции - анионов определяет избирательный характер поглощения из раствора анионов платин. [15]
Страницы: 1 2 3 4 5