Поверхность - оксид - алюминий
Cтраница 3
Прокаливание при более низких температурах приводило к избытку гидроксильных групп на поверхности оксида алюминия, что в свою очередь сопровождалось при хлорировании образованием большого количества хлороводорода и синтезом малоактивного катализатора, содержащего мало хлора. При более высоких температурах прокаливания снижение изомеризующей активности связано с уменьшением удельной поверхности оксида алюминия. Гидрирующая активность практически не зависела от условий термообработки. [31]
Используют также молибденовый катализатор, представляющий собой оксид молибдена, нанесенный на поверхность оксида алюминия. [32]
Результаты исследований методом ИК-спектроскопии [172] указывают на сложный характер взаимодействия ОСС с поверхностью оксида алюминия. Экспериментальные данные свидетельствуют о физической адсорбции ОСС, образовании водородных и координационных связей и возможности химических реакций. [33]
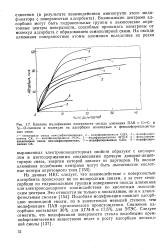
Под воздействием водяных паров, содержащихся в газосырьевой смеси, происходят гидролиз связанного с поверхностью оксида алюминия хлора и его удаление из зоны катализа в виде хлорида водорода, вследствие чего кислотность катализатора уменьшается. Скорость этого процесса определяется в основном концентрацией водяннх паров в зоне катализа. На рис. 3 показано снижение активности катализатора АП-64 в процессе дехлорирования при различной влажности и температуре 4Э0 С. Октановое число риформата ( при неизменной температуре) снизилось при содержании воды в водородсодержащем газе 400 млн. на 7 пунктов за четверо суток, причем понижение октанового числа началось практически сразу после аварийного повышения влажности. [34]
В работе [77] описаны закономерности формирования ряда промышленных катализаторов, в частности полученных нанесением платины на поверхность оксида алюминия. [35]
Есть определенные доказательства в пользу того, что частично диссоциированные хлориды образуют более прочные связи с поверхностью оксида алюминия, чем можно было бы ожидать в результате простой физической адсорбции. Скорость формирования таких связей низка и ощутимых значений она достигает только на адсорбентах, проработавших несколько лет. При таком роде взаимодействия HCI нельзя удалить продувкой горячим газом, хотя при пропарке хлороводород будет все-таки удален с поверхности оксида алюминия. Таким образом, адсорбция на оксиде алюминия является обратимой. [36]
С другой стороны, Де Буром было отмечено [ НЗа ], что удаление слоев воды с поверхности оксида алюминия происходит в виде отчетливо выраженных ступенек. [37]
Гидратация активных центров поверхности оксида алюминия и ионизация поверхностных гидроксилов с отщеплением протона приводят к появлению у поверхности оксида алюминия электрического заряда, величина которого существенно зависит от рН, так как Н - и ОН - - ионы являются потенциалопределяющими ионами поверхности. Знак заряда поверхности изменяется в границах рН 7 - 9, и потому оксид алюминия является ионообменни-ком амфотерной природы. [38]
Исследование влияния природы кислоты на обменную емкость 7-оксида алюминия показало, что ионный обмен сопровождается нейтрализацией гидроксильных групп на поверхности оксида алюминия. [39]
В связи с тем, что десорбция H2S и SO2 с поверхности диоксида титана протекает значительно легче, чем с поверхности оксида алюминия, сделан вывод об отсутствии сильного сульфатирования в первом случае, что позволяет использовать диоксид титана в качестве более эффективного катализатора процесса Клауса, чем обычно применяемый для этой цели оксид алюминия. [40]
Основным промышленным катализатором процесса риформинга является алюмоплатиновый катализатор ( 0 3 - 0 8 % масс, платины, нанесенной на поверхность оксида алюминия); в последние годы наряду с платиной на основу наносится рений. Применение более активного биметаллического платинорениевого катализатора позволяет снизить давление в реакторе с 3 - 4 до 0 70 - 1 4 МПа. Используют также молибденовый катализатор, представляющий собой оксид молибдена, нанесенный на поверхность оксида алюминия. Катализатор имеет форму цилиндров диаметром 2 6 мм и высотой 4 мм. [41]
 |
Влияние модификации поверхности оксида алюминия ПАВ с С-С - и Si-О - связями в молекуле на адсорбцию эпоксидных и фенолрформальдегид. [42] |
Из данных ИКС следует, что взаимодействие с поверхностью адсорбента происходит не по водородным связям, а за счет хемо-сорбции по гидроксильным группам поверхности оксида алюминия или электронодонорного взаимодействия по кислотным льюисов-ским центрам. Подобная модификация снижает адсорбцию эпоксидной смолы, но в значительно меньшей степени, чем модификация ПАВ органического происхождения. Снижение адсорбции составляет 30 % для АГМ-9 и 17 5 % для ЭТЭС. [43]
 |
Влияние природы хлорагента на изомеризующую активность хлорированного тт-оксида алюминия.| Влияние среды при хлорировании катализаторов на их активность в реакции изомеризации - бутана. [44] |
Изменение природы хлорагента практически не влияло на содержание хлора в образцах катализатора; это приводит к заключению, что в состав активных центров поверхности оксида алюминия, ответственных за реакцию изомеризации, входит лишь небольшая часть от общего содержания хлора в катализаторе. Суммарный баланс хлорирования указывает на замену ионов кислорода поверхности оксида алюминия ионами хлора. Эта реакция является основной при хлорировании. Определяющее влияние природы хлорорганического соединения на активность катализатора в реакции изомеризации может быть объяснено необходимостью фиксации двух ионов хлора на поверхности оксида алюминия на определенном расстоянии друг от друга. [45]
Страницы: 1 2 3 4 5