Неравновесный раствор
Cтраница 3
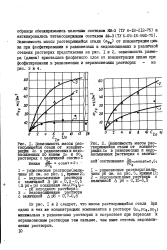
Из рис. I и 2 следует, что масса растворяющейся стали при одних и тех же концентрациях компонентов в растворе ( zn p04 NO) минимальна в равновесных растворах и возрастает при переходе к неравновесным растворам тем сильнее, чем выше степень недонасы-щения растворов. [32]
 |
Схема образования капиллярно-пористой структуры пленок. [33] |
При прохождении процесса образования пористой структуры через стадию студнеобразования и допущении, что из-за различий в подвижности макромолекул и молекул растворителя фазовый распад проходит за счет преимущественного выделения низкомолекулярной фазы ( низкомолекулярные компоненты системы с незначительным содержанием полимера) из неравновесного раствора с формированием полимерной фазы в виде каркаса, процесс возникновения капиллярно-пористой структуры пленочных фильтров можно представить следующим образом. [34]
Согласно этой гипотезе система ( раствор полимера) при переводе ( путем изменения температуры или состава растворителя) в неравновесное состояние распадается на две фазы, причем низкоконцентрированная фаза выделяется из неравновесного раствора в виде изолированных микроучастков, постепенно обедняя этот неравновесный раствор растворителем. Эта каркасная фаза и определяет основные механические свойства студня. [35]
При образовании мартенсита из аустенита, что связано с переходом у-железа, в котором растворимость углерода высока ( 2 %) в а-железо, в котором равновесная растворимость углерода крайне низка 0 01 %), весь содержавшийся в аустените углерод фиксируется в сс-железе, образуя сильно пересыщенный неравновесный раствор. Такое пересыщение а-твердого раствора углеродом приводит к сильным искажениям кристаллической решетки а-железа, сдвигам в атомных плоскостях, и, как следствие, к созданию высокой плотности дислокаций. [36]
Изменение степени насыщенности форматирующего раствора вызывает изменение фазового состава слоев. В неравновесных растворах фосфатные слои обогащены солями железа по сравнению с фосфатными слоями, сформированными в равновесных растворах. [37]
При достаточно большой концентрации ОН ( ао) сульфат алюминия гидролизуется непосредственно до А1 ( ОН) а со структурой гидрар-гиллита. При этом в неравновесном растворе, каким является очищаемая вода, неизбежно будут присутствовать мономеры и димеры алюминия, которые образуются еще на стадии приготовления рабочих растворов. Эти аквагидроксокомплексы хемосорбируются на поверхности частиц гидроксида алюминия, сообщая последним соответствующий заряд. Поэтому в дисперсной системе могут присутствовать частицы, характеризующиеся различными дисперсностью и величиной заряда. В результате протекания реакции гидролиза на поверхности происходит нейтрализация заряда, что способствует коагуляции частиц. [38]
Кроме методики измерения и критериальных величин необратимой деформации ( вязкости), принятой для оценки температур плавления ( застудневания), важную роль в гистерезисных явлениях играет степень завершенности установления равновесных фаз по составу. Уже отмечалось, что завершающая стадия распада исходного неравновесного раствора на равновесные фазы протекает очень медленно, поскольку происходит выравнивание химических потенциалов компонентов в сосуществующих фазах. Поэтому те характеристики, которые обусловлены особенностями матричной фазы, и в первую очередь механические свойства, в свежеобразованных студнях будут отличаться от характеристик для студней, выдержанных во времени. [39]
Установлено, что при температурах перехода ив истинного раствора в дисперсный Ти структура битумов представляет со бой насыщенный равновесный раствор асфальтенов в смолисто-углеводородных компонентах. Выше Ти структура битумов явля - ется ненасыщенным равновесным раотвороМ а ниже Ти-пересы-щенным неравновесным раствором. [40]
II были рассмотрены два возможных шути превращения в зависимости от соотношения скоростей роста обеих фаз. В пределе такая схема распада на фазы пред ставляет собой постепенное обеднение исходного неравновесного раствора растворителем ( отделение пер вой фазы) и достижение в конце концов раствором равновесной концентрации, отвечающей составу второй фазы. При этом неравновесный исходный раствор, превращающийся в равновесную вторую фазу, остается пространственно непрерывным, а быстро возникающие и растущие зародыши первой фазы оказываются как бы диспергированными в непрерывном остове. [41]
Из-за высокой вязкости концентрированной фазы гидростатическое перемещение, встреча и слияние частиц изолированной низкоконцентрированной фазы оказываются практически невозможными несмотря на то, что при относительно невысоких концентрациях исходного раствора суммарный объем второй ( матричной) фазы невелик и, следовательно, пространства, разделяющие частицы низкоконцентрированной фазы, могут быть очень малыми. Только при пониженных концентрациях исходного раствора, когда объем образующейся при распаде неравновесного раствора полимерной фазы становится очень малым, может произойти механическое разрушение матрицы, и включенные в нее частицы первой фазы частично сольются в единый слой. [42]
Неравновесный раствор, из которого образуется матричная фаза в результате удаления растворителя ( расходуемого на образование низкоконцентрированной фазы) подходит к равновесному состоянию медленно, причем тем медленнее, чем ближе это равновесное состояние. Та-жим образом, должен наблюдаться гистерезис температур застудневания, так как в принципе эти температуры соответствуют точкам перехода неравновесного раствора в нетекучее состояние, а концентрация этого раствора лишь постепенно приближается к концентрации равновесной полимерной фазы. [43]
Это следует из сопоставления кинетической подвижности низкомолекулярных веществ и полимерных молекул. Тогда вторая фаза будет иметь равновесный состав не за счет обособления и разрастания частиц этой фазы, а за счет постепенного обеднения неравновесного раствора растворителем, который отделяется в виде первой фазы. С точки зрения термодинамики оба пути возможны, если они приводят к равновесным составам фаз. Но при допущении указанного различия в скоростях образования и роста зародышей первой фазы становится понятным возникновение пространственных структур, остовом которых япляется полимерная фаза. [44]
 |
Диаграмма состояния для системы полимер ( П - - два растворителя ( Pi и Р.. Пояснения в тексте. [45] |
Страницы: 1 2 3 4 5