Растворение - углеводород
Cтраница 1
 |
Изменение термодинамических параметров при переносе углеводородов из неполярной среды в воду. [1] |
Растворение углеводородов в воде приводит к уменьшению энтропии системы в результате увеличения доли упорядоченных элементов в структуре воды. Поэтому удаление молекул углеводорода из воды ( переход их в неполярное окружение) сопровождается увеличением энтропии и переходом системы в более выгодное энергетическое состояние. [2]
Растворение углеводорода в воде можно трактовать как внедрение неполярных молекул в структурированные ( льдоподобные) области воды и в более плотные неструктурированные области. В первом случае неполярные молекулы размещаются в пустотах рыхлой структуры, образуя клатраты, причем дополнительные контакты молекул с водой приводят к уменьшению энергии. Во втором случае увеличение числа контактов углеводород - вода приводит к уменьшению числа контактов вода - вода, которым отвечает более низкая энергия. В результате энтальпия увеличивается. Углеводороды лучше растворяются в структурированных областях и равновесие сдвигается в сторону увеличения структурированности ( образование айсбергов), что означает понижение энтропии. В целом антипатия углеводородов и воды определяется большим выигрышем свободной энергии при контактах вода-вода, чем при контактах углеводород - вода. [3]
Теория растворения углеводородов в избирательных растворителях дает объяснение разнообразию критических температур растворения ( КТР) углеводородов. [4]
Величины теплоты растворения углеводородов С в водном растворе фурфурола, используемые в тепловых расчетах, даны в указанных работах Жордана и др. и Велти и др. Эти величины составляют 35 - 40 % от теплоты испарения углеводородов С. [5]
Критическая температура растворения углеводородов в S02 Зависит от химического состава их и молекулярного веса. [6]
Анализируя процесс растворения углеводородов в полярных растворителях, мы можем отметить, что при относительно низких температурах происходит избирательное растворение углеводородов, преимущественно непредельных и ароматического ряда. При повышенных температурах за пределами критической температуры растворения растворитель и углеводороды образуют однородную смесь. [7]
Газохроматографическое определение термодинамических характеристик растворения углеводородов и спиртов в некоторых растворителях. [8]
АНИЛИНОВАЯ ТОЧКА - критическая т-ра растворения углеводорода или смеси углеводородов в анилине. Для характеристики индивидуальных углеводородов применяются два способа определения А. Минимальную т-ру, при к-рой анилин смешивается во всех концентрациях с углеводородом, называют максимальной А. [9]
Так, нафталин сульфируется при растворении углеводорода в моногидрате преимущественно в а-положение. [10]
Вообще говоря, кислотность снижается из-за растворения углеводородов ( в том числе полимеров), бутилсульфатов и воды в кислоте. [11]
Таким образом, природа сил, обусловливающих растворение углеводородов в водных растворах мыл ниже ККМ и гидротропного агента - бу-тирата натрия, одинакова, о чем свидетельствует близкий порядок величин теплот растворения углеводородов в этих растворах, зависящий только от природы углеводорода. [12]
Таким образом, и в данном случае растворение углеводородов протекает преимущественно за счет соединений с меньшим молекулярным весом. [13]
Не менее характерной константой является критическая температура растворения углеводородов в анилине. [14]
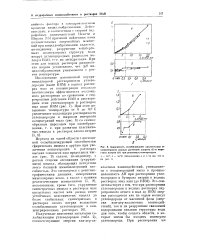 |
Зависимость солюбилизации циклогексана от концентрации водных растворов лаурата ( I и мири-стата натрия ( II при различных температурах. [15] |
Страницы: 1 2 3 4