Растворимость - поваренная соль
Cтраница 2
Таким образом величина произведения растворимости поваренной соли превышена, и хлористый натрий выпадает из раствора. [16]
 |
Кривые растворимости в воде некоторых солей. [17] |
Из графика видно, что растворимость поваренной соли NaCl мало изменяется с повышением температуры, так как кривая ее растворимости располагается почти горизонтально. Наоборот, растворимость нитрата калия в большой степени зависит от температуры. [18]
 |
Влияние температуры на растворимость газов.| Кривые растворимости в воде некоторых солей. [19] |
Из графика видно, что растворимость поваренной соли NaCl мало изменяется с повышением температуры, так как кривая ее растворимости располагается почти горизонтально. Наоборот, растворимость нитрата калия в большой степени зависит от температуры. Растворимость сульфата натрия растет лишь до 32 С, а при дальнейшем повышении температуры она уменьшается. [20]
 |
Кривые растворимости в воде некоторых солей. [21] |
Из графика видно, что растворимость поваренной соли NaCl мало изменяется с повышением температуры, так как кривая ее растворимости располагается почти горизонтально. Наоборот, растворимость нитрата калия в большой степени зависит от температуры. [22]
При какой температуре растворимость калиевой селитры равна растворимости поваренной соли. [23]
В присутствии Других солей ( хлоридов, сульфатов) растворимость поваренной соли снижается. [24]
В процессе выпарки электролитических щелоков по мере роста концентрации щелочи растворимость поваренной соли уменьшается и она выпадает в осадок. [25]
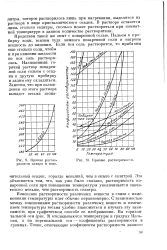 |
Кривая растворимости сахара в воде.| Кривые растворимости. [26] |
Это объясняется тем, что, как уже было сказано, растворимость поваренной соли при повышении температуры увеличивается значительно меньше, чем растворимость селитры. [27]
В присутствии хлоридов калия, кальция и магния, щелочи и соляной кислоты растворимость поваренной соли уменьшается ( см. Приложение III, стр. [28]
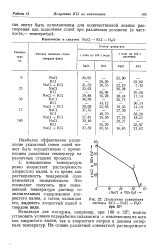 |
Диаграмма равновесия. [29] |
С повышением температуры резко возрастает растворимость хлористого калия, в то время как растворимость поваренной соли изменяется незначительно. Это позволяет получить при повышенной температуре раствор со значительным содержанием хлористого калия, а затем, охлаждая его, выделить хлористый калий в твердом виде. [30]
Страницы: 1 2 3 4 5