Растворимость - поваренная соль
Cтраница 3
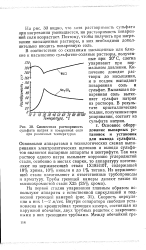 |
Совместная растворимость. [31] |
На рис. 30 видно, что хотя растворимость сульфата при нагревании уменьшается, но растворимость поваренной соли возрастает. Поэтому, чтобы получить при нагревании насыщенные растворы, в них необходимо дополнительно вводить поваренную соль. [32]
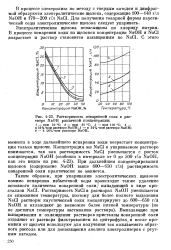 |
Растворимость поваренной соли в растворе NaOH различной концентрации. [33] |
При дальнейшем концентрировании щелоков ( содержание NaOH выше 600 - 650 г / л) растворимость поваренной соли практически не меняется. [34]
Это отрицательно влияет на - процесс электролиза, так как в присутствии значительного количества сульфатов ухудшается растворимость поваренной соли и не удается получить рассол, содержащий более 300 г / л NaCl; кроме того, заметно увеличивается износ анодов. Поэтому вывод сульфатов из цикла совершенно необходим. [35]
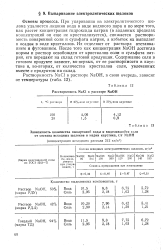 |
Растворимость NaCi в растзоре NaOH. [36] |
При упаривании из электролитического ше-лока удаляется лишняя вода в виде водяного пара и по мере того, как растет концентрация гидроксида натрия ( в заданных пределах концентраций он еще не кристаллизуется), снижается растворимость поваренной соли и сульфата натрия, а избыток их выпадает в осадок в виде кристаллов. Их отделяют от раствора отстаиванием и фугованием. После того как концентрация NaOH достигла нормы и раствор освобожден от кристаллов соли и сульфата натрия, его передают на склад готовой продукции. Содержание соли в готовом продукте зависит, во-первых, от ее растворимости в каустике и, во-вторых, от количества кристаллов соли, увлеченных вместе с продуктом на склад. [37]
Растворимость поваренной соли в растворах едкого натра с повышением концентрации NaOH уменьшается ( рис. 20 - 3), поэтому в процессе выпаривания электролитической щелочи из раствора выделяется в твердом виде около 98 % NaCl. Растворимость поваренной соли в растворах едкого натра уменьшается также с понижением температуры раствора ( см. рис. 20 - 3), вследствие чего упаренный раствор щелочи охлаждают: при этом кристаллизуется дополнительное количество NaCl и улучшается качество каустической соды. [38]
Щелочь, полученная в диафрагменных ваннах, содержит 110 - 120 г / л NaOH и 180 - 170 г / л NaCl. Растворимость поваренной соли с увеличением концентрации NaOH в растворе падает. [39]
На рис. 3 показана зависимость растворимости некоторых солей в воде от температуры. Кривая растворимости поваренной соли NaCl приближается к горизонтальной прямой и поэтому считают, что растворимость ее в воде не зависит от температуры. [40]
Влияние этого фактора особенно наглядно иллюстрируется некоторыми месторождениями в Пенсильвании, где иногда концентрация солей в пластовой воде достигает таких пределов, что происходит засорение скважины вследствие кристаллизации в ней значительных количеств поваренной соли. Так как растворимость поваренной соли мало зависит от температуры, то причина ее массового выпадения заключается, очевидно, в удалении части растворителя вследствие его испарения. [41]
Влияние этого фактора особенно наглядно иллюстрируется некоторыми месторождениями в Пенсильвании, где иногда концентрация солей в пластовой воде достигает таких пределов, что происходит засорение скважины вследствие кристаллизации в ней. Так как растворимость поваренной соли мало зависит от температуры, то причина ее массового выпадения заключается, очевидно, в удалении части растворителя вследствие его испарения. [42]
Охлаждение каустической соды перед транспортировкой в бак готовой продукции необходимо для уменьшения потерь соли NaCl с каустиком и улучшения качества последнего. Известно, что растворимость поваренной соли в растворах едкого натра уменьшается с понижением температуры. [43]
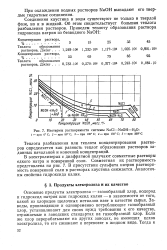 |
Изотермы растворимости системы NaCl-NaOH-РЬО. [44] |
В электролизерах с диафрагмой получают совместные растворы едкого натра и поваренной соли. В присутствии сульфата натрия растворимость поваренной соли в растворах каустика снижается. Аналогичны свойства гидроксида калия. [45]
Страницы: 1 2 3 4 5