А-протон
Cтраница 2
Однако, поскольку и а-протон легко. Так, реакция цис - и игранс-р-хдорстирола с фениллитием, приводящая к образованию фенилацетилена, имеет кинетический изотопный a - H / D-эффект 15 для транс-соединения и 8 для уцс-соединения. Осуществляется ли подобный механизм и с менее сильными основаниями, чем фениллитий - неизвестно. [16]
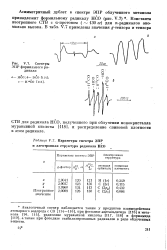 |
Параметры спектра ЭПР и электронная структура радикала НСО. [17] |
Константа изотропного СТВ с а-протоном ( - 130 ее) для я-радикалов аномально высока. [18]
 |
Диаграмма потенциальной энергии конформационных переходов монозамещенных цик-логексанов.| Конформационная энергия нитрогруппы. [19] |
Ошибка в измерении ширины пика а-протона может. [20]
Поскольку I образуется путем отрыва более реакционноспособного а-протона, а II - менее реакционноспособного / 8-протона, можно предполагать, что для образования II требуются более сильные основные центры; для образования I достаточно наличия более слабых центров. Оба ряда относительных величин находятся в разумном соответствии. Таким образом, селективность, т.е. отношение выходов I / II, регулируется основной силой катализаторов. Здесь интересно отметить, что отношения I / II и транс / цис больше единицы в случае твердых основных катализаторов, но на кислотных катализаторах типа алюмосиликатов, окиси алюминия, алюмоборатов, сульфатов и т.п. отношение транс / цис меньше единицы, a I / II много меньше единицы. [21]
Сигнал в слабом поле приписывают а-протонам; большое дублетное расщепление ( 47 0 Гц) обусловлено геминальным спин-спиновым взаимодействием 1На - 19F, а меньшее расщепление - вицинальным спин-спиновым взаимодействием На-Пр. Триплетное расщепление сигналов р-протонов обусловлено спин-спиновым взаимодействием JHp - 19F ( константа равна 20 Гц), но дальнейшего расщепления компонентов триплета, ожидаемого в случае вицинального спин-спинового взаимодействия протонов, не наблюдается. [22]
В плоском радикале СТВ с а-протонами имеет отрицательный знак [118] и по мере деформации радикала увеличивается. [23]
С кетонами, содержащими два типа а-протонов, может образоваться смесь изомерных комплексов. Такая картина наблюдается в случае метилэтилкетона и ацетонилацетона, но не для метилизопропилкетона. ПМР-спектры кетонных комплексов типа 10, растворенных в ацетоне - He или других кетонах, не показывают наличия обмена с растворителем. [24]
При этом за счет отщепления одного а-протона образуется С С связь, а за счет отщепления второго а-протона - Pd С. При гидрировании комплекса Pd С CHR образуется насыщенное соединение, содержащее четыре атома изотопа. [25]
Фудзивара и Флори [11] рассчитали спектр а-протонов полистирола, учитывая конформацию цепи и экранирование, обусловленное кольцевыми токами. [26]
СТС обусловлена в основном СТВ с а-протоном, jj - протонами группы R и ядром N. Этот вывод согласуется с составом конечных продуктов [170-173]: во всех аминах с большим выходом образуются димеры R R NC ( R) H-C ( R) HNR R, которые, очевидно, являются продуктами рекомбинации ос-амин-алкильных радикалов. [27]
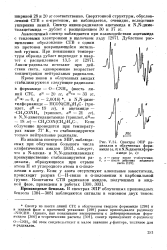 |
Спектры ЭПР радикалов в облученных формамиде ( а, б и 1 Н - диметилформ-амиде ( в, г. [28] |
Сверхтонкой структуры, обусловленной СТВ с а-протоном, не наблюдается, очевидно, вследствие ушйрения линий. [29]
Приведенные примеры еще раз подчеркивают важность отщепления а-протона и тем самым глубокое различие между диазоалканами и солями диазония. [30]
Страницы: 1 2 3 4 5