Пятикоординационный комплекс
Cтраница 2
Есть пятикоординационные комплексы с искаженной геометрической формой, например транс-аква-бис ( 8-гидроксихинолин) цинк [29], который имеет строение, промежуточное между формами ТБП и КП. [16]
Все пятикоординационные комплексы, такие, как комплекс (24.11), лепко присоединяют шестой лиганд и приобретают октаэдр ическую конфигурацию. [17]
Наличие стабильных пятикоординационных комплексов с конфигурацией ds позволяет предположить, что четырех-координационные комплексы являются координационно-ненасыщенными и что поэтому в реакциях замещения будет преобладать такой механизм, который приводит к временному увеличению координационного числа центрального атома. Образование пяти эквивалентных связей приводит к 18-электронной ( 10 связывающих и 8 несвязывающих электронов) валентной оболочке, типичной для ближайшего инертного газа. [18]
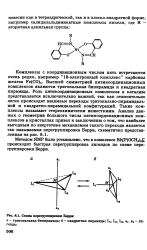 |
Схема перегруппировки Берри. [19] |
Высшей симметрией пятикоординационных комплексов являются тригональная бипирамида и квадратная пирамида. Роль пятикоординационных комплексов в катализе представляется исключительно важной, так как относительно легко происходят взаимные переходы тригонально-пирамидаль-ной и квадратно-пирамидальной конфигураций. Такие комплексы называют стереохимически нежесткими. [20]
Оптическая изомерия пятикоординационных комплексов встречается реже. [21]
Простейшим примером пятикоординационного комплекса служит ( РеСЦ) 2; результаты спектроскопических исследований ( ИК-спектры, спектры комбинационного рассеяния) [ 8а ] соединения ( CgHisN2) 2 ( FeCl5) 2 - доказывают, что он имеет триго-нально-бипирамидальное строение. [22]
Замещение в пятикоординационных комплексах изучено еще недостаточно хорошо. Оно может проходить как по диссоциативному, так и по ассоциативному механизмам. [23]
Замещение в пятикоординационных комплексах изучено еще недостаточно, Оно может проходить как по диссоциативному, так и по ассоциативному механизмам. [24]
Существуют квадратные или пятикоординационные комплексы. [25]
Здесь были найдены настоящие пятикоординационные комплексы. [26]
В отличие от пятикоординационных комплексов, семикоорди-национные, найденные в двух родственных соединениях - [ FeA ( H20) 20 ] ( C104) 4 и [ FeA ( NCS) 2 ] ClO4, где А C15H23N5 - несомненно являются вынужденными. Пентагонально-бипира-мидальная форма комплексов определяется строением пентаден-татного органического лиганда ( см. рис. 60 и 61, стр. [27]
Во всех этих пятикоординационных комплексах в отличие от аналогичных комплексов Rh111 и Ir111 ( и квадратных комплексов Rh1 и Ir1) суммарное число электронов на валентных МО равно не 16, а 18; при этом соблюдается общее правило, хгфактерное для низкоспиновых тетрагонально-пирамидальных комплексов металлов с электронной конфигурацией dB: атом металла смещен из основания пирамиды к ее вершине на 0 2 - 0 3 А, а связь М - L, направленная к вершине пирамиды, существенно слабее связей с лигандами, расположенными в ее основании. В RhCl ( C4H6) 2 расстояние Rh - С1 равно 2 45 А, в RhCl ( CO) ( PPh3) 2SO2 расстояние Rh - SO2 2 45 А, а в IrCl ( CO) ( PPh3) 2SO2 Ir-S 2 49 А. [28]
Одну из них составляют пятикоординационные комплексы. [29]
 |
Схема перекрывания орбиталей по ст - и я - типу в плоскоквадратном комплексе. [30] |
Страницы: 1 2 3 4 5