Пятикоординационный комплекс
Cтраница 4
Она включает разности заселенностей перекрывания отдельных связей и орбиталей при переходе от четырехкоординационного комплекса плоскостного типа к пятикоординационному комплексу бипирамидального типа. Эта разница показывает, что при переходе от Н20 к Ш - ослабляются все связи и примерно в одинаковой мере. Связь Pt - С1, лежащая в плоскости, в основном состоянии отсутствует. Поэтому в табл. 20 фактически для нее приведена не разность, а сама заселенность перекрывания в переходном состоянии. Причем это различие полностью относится к взаимодействию Pt ( 6s) - L и Pt ( 4км / 2) - L. Сумма этих ослаблений почти одинакова в обоих случаях. [46]
Представляют интерес механизмы взаимного перехода геометрических форм, так как они позволяют интерпретировать протекание многих реакций с участием пятикоординационных комплексов. Для перехода от формы ТБП к форме КП требуются небольшие перемещения лигандов в пространстве ( см. разд. Так, известны / две соли с пентацианоникко-лат ( П) - ионом и содержащими один и тот же центральный атом и бидентатные лиганды катионами. В водном растворе строение иона [ Ni ( CN) 5 ] 3 -, по-видимому, также квадратно-пирамидальное. [47]
Берри [313] предлагает механизм изомеризации в этих системах, которой, по-видимому, объясняет многие особенности динамических эффектов в пятикоординационных комплексах. [48]
Для d10 - ионов металла с положительным зарядом на центральном атоме углерода нуклеофильная атака, очевидно, возможна f поскольку существуют пятикоординационные комплексы этих металлов. [50]
В соответствии с результатами структурных исследований ( см. рис. Ill А) для пятикоординационных комплексов Д - Т1С14 принята конфигурация тетрагональной пирамиды, для пятикоординационных комплексов Д-5 пХ4 - конфигурация тригональной бипирами-ды, для шестикоординационных комплексов тетрагалогенидов титана и олова - конфигурация октаэдра. [51]
Единственным соединением, исследованным структурно, является ( РРпзМе) з [ Р1: ( 8пС1з) 5 ] - В кристаллах этого соединения найдены мономерные пятикоординационные комплексы [ Pt ( SnCl3) 5 ] 3 -, в которых связи Pt-Sn направлены к вершинам тригональной бипирамиды. Расстояния Pt-Sn равны 2 54 А. Это, насколько нам известно, первый пример координационного числа 5 в соединениях Pt11 с монодентатными лиган-дами. [52]
Высшей симметрией пятикоординационных комплексов являются тригональная бипирамида и квадратная пирамида. Роль пятикоординационных комплексов в катализе представляется исключительно важной, так как относительно легко происходят взаимные переходы тригонально-пирамидаль-ной и квадратно-пирамидальной конфигураций. Такие комплексы называют стереохимически нежесткими. [53]
В случае бромида удается выделить пятикоординационный неустойчивый комплекс [ ( Ph2P) 2PtBr ( CNMe) 2 ] Br, который легко теряет изонитрил, превращаясь в, ионный комплекс [ ( PhaP) 2PtBr ( CNMe) ] Br. В случае иодида пятикоординационный комплекс является единственным продуктом реакции. [54]
Оба атома рутения в димерной молекуле имеют октаэдрическое окружение и связаны между собой тройным хлорным мостиком. Среднее расстояние Ru - Р ( 2 329) сравнимо с длинами аналогичных связей в пятикоординационных комплексах ( см. реф. Среднее значение длины связи Ru - Cl не-мостнкового типа равно 2 35 А, как и в большинстве комплексов трехвалентного рутения. [55]
Комплексы Pt ( II) интенсивно исследовались главным образом потому, что они довольно устойчивы и реакции с их участием протекают достаточно медленно, чтобы можно было следить за кинетикой обмена лигандов. Авторы работы [7] показали, что реакция ( 4) протекает по механизму 5к2 и включает стадию образования промежуточного пятикоординационного комплекса. [56]
 |
Строение катиона хлоро этиленбис ( дифенилфосфин кобальта ( П, содержащегося в красной ( а и зеленой ( б модификациях его твердых солей.| Строение фосфиновых. [57] |
Для конфигураций d8, d9 и d10 порядок устойчивости становится обратным. К сожалению, имеется небольшое число данных для проверки этих обобщений, однако известно, что для центральных атомов с конфигурацией d8 пятикоординационные комплексы, например, [ Fe ( CO) 5 ], имеют форму ТБП. Очевидно, что небольшая энергия стабилизации поля лигандов, благоприятствующая форме КП, компенсирует свойственное форме ТБП стерическое преимущество, что позволяет выделить оба комплекса. В растворе обе формы легко переходят одна в другую посредством псевдоьращения по Берри или в результате диссоциации с последующей рекомбинацией ( см. разд. [58]
 |
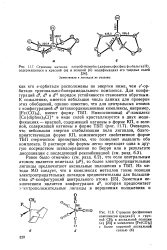
Тригональная бипирамида с экваториальными лигандами, смещенными в сторону атома водорода. Расстояние от атома металла до плоскости экваториальных лигандов обозначено d. [59] |
Почти во всех кристаллических структурах гидридных комплексов переходных металлов лиганды, смежные с координированным гидрид-ионом, смещены в его сторону; степень этого искажения колеблется. Такое искажение наблюдается также в четырех - и шестикоординационных комплексах, но в этих случаях его труднее оценить количественно, чем для пятикоординационных комплексов. Три экваториальных атома определяют плоскость, а расстояние, на котором центральный атом находится от этой плоскости, можно принять за меру искажения. [60]
Страницы: 1 2 3 4 5
