Окись - пиридин
Cтраница 1
Окись пиридина является важным исходным продуктом при получении многих производных пиридина, замещенньих в 4, 3, 2 положениях. [1]
Окись пиридина гладко восстанавливается до пиридина при 25, но дальнейшее восстановление требует более высокой температуры. Нитросоединения и ароматические галогениды не восстанавливаются. [2]
Окиси пиридина и его производных были использованы при решении вопроса об ориентации заместителей. Так, хотя пиридин нитруется в положение 3, его N-окись дает главным образом 4-изомер. Этот метод позволяет синтезировать 4-нитропроизводные, поскольку окись может быть восстановлена обратно в пиридин. [3]
Окись пиридина значительно более способна к электрофиль-ным замещениям, чем пиридин. [4]
Окись пиридина гладко восстанавливается до пиридина при 25, но дальнейшее восстановление требует более высокой температуры. Нитросоединения и ароматические галогениды не восстанавливаются. [5]
Окись пиридина значительно более способна к электрофиль-ному замещению, чем пиридин. Например, нитрат калия в дымящей серной кислоте при 100 С дает 90 % - ный выход N-окиси 4-нитро-пиридина. [6]
Окись пиридина подвергается электрофильному и ну-клеофильному замещению легче, чем бензол. Объясните, б) Объясните, почему так же ведет себя и нитрозобензол. [7]
Окиси пиридина могут вступать в ряд реакций, которые еще не обсуждались, но которые имеют большое значение. Как указывалось, N - Ю - связь N-окиси пиридина стабилизована и, следовательно, можно ожидать, что она будет относительно устойчива к восстановлению. Действительно, оказалось, что многие заместители могут быть избирательно восстановлены в присутствии N-окисной группы. [8]
Окись пиридина сульфируется в жестких условиях ( H2SO4 - SOs - Hg2, 230) с образованием 3-сульфокислоты ( ср. [9]
Сама окись пиридина в растворах в неполярных растворителях поглощает при 1270 см 1, но частота поглощения, по-видимому, очень чувствительна к электрическим свойствам замещающих групп. Ме: тис - Ноел, Вольф и Галле [55] исследовали несколько окисей третичных аминов. Это очень большое смещение по сравнению с соответствующим поглощением у пиридинового ряда, но в тех случаях, когда кратность связи становится минимальной, можно ожидать сдвига полосы поглощения в более низкочастотную область спектра. [10]
В окиси пиридина, однако, в момент атаки элек-трофильного реагента в а - или 7 положение возможна перестройка электронной системы по схемам, приведенным в трех формулах справа: кислород примыкает двойной связью к азоту за счет перемещения одной л-пары электронов к а - или у - УглеР ДУ, благодаря чему становится возможным а - или у-электрофильное замещение. Так, нитрование с выходом, близким к количественному, проходит в - положение. Кислород может быть затем удален восстановителями. Путем восстановления у-нитропиридина легко получить у-аминопиридин. [11]
В окиси пиридина, однако, в момент атаки электро-фильного реагента в а - или - положение возможна перестройка электронной системы по схемам, приведенным в трех формулах справа: кислород примыкает двойной связью к азоту за счет перемещения одной я-пары электронов к а - или у-углероду, благодаря чему становится возможным а - или у-электрофильное замещение. Так, нитрование с выходом, близким к количественному, проходит в у-положение. Кислород может быть затем удален восстановителями. Путем восстановления у-нитропиридина легко получить у-аминопиридин. [12]
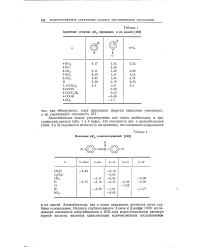 |
Сравнение величин р / Са пиридинов и их окисей. [13] |
Азоксибензолы, как и окиси пиридинов, являются очень слабыми основаниями. [14]
Переход от Л - окиси пиридина последовательно к окисям хино-лина, акридина и феназина облегчает их восстановление; в той же последовательности уменьшается дипольный момент этих молекул, что позволило предположить [162] наличие определенной связи между этими величинами. [15]
Страницы: 1 2 3