Большинство - органическая молекула
Cтраница 2
Известно, что в большинстве органических молекул электроны сгруппированы попарно в молекулярных орбитах о, тг или в р-орбитах атомов с неподеленными электронами. В спектроскопии состояние молекул, содержащих только такие спаренные электроны с антипараллельным спином, называется синглетнъш состоянием, а состояние, в котором молекула содержит два неспаренных электрона с параллельным спином, называется триплетным состоянием. [16]
Давно уже отмечено, что большинство органических молекул состоит из двух частей: фрагмента, который в ходе реакции остается без изменения, и группы, подвергающейся при этом превращениям. Атом или группу атомов, связанных определенным образом, наличие которых в молекуле органического вещества придает ему характерные свойства, называют функциональной группой. [17]
При умеренных температурах в отсутствие катализаторов большинство органических молекул с молекулярным водородом не реагирует. На многих металлических катализаторах уже при температурах порядка - 100 этилен быстро гидрируется до этана. При температурах выше 150 в присутствии никелевых, кобальтовых или железных катализаторов может протекать гидрокрекинг этилена до метана. Выше 150 на этих катализаторах может протекать гидрокрекинг но только этилена, но и других олефиновых и парафиновых углеводородов. В соответствующих условиях ( давление и температура) почти все углеводороды и органические соединения, содержащие кислород или азот, в присутствии никелевых или других катализаторов могут претерпевать гидрирование или гидрокрекинг. [18]
К сожалению, некоторые члены уравнения (4.2) для большинства органических молекул неизвестны. В особенности это относится к энергии нулевых колебаний атомов, которая по абсолютной величине значительно превышает небольшие разности, связанные с изменениями геометрии молекул: так, инкремент нулевой энергии на СН2 - группу в алканах составляет 17 7 ккал / моль. Эти изменения обычно несколько больше точности лучших термохимических измерений и потому в ряде случаев учет энергии нулевых колебаний целесообразен. Из сказанного следует, что построение аддитивных схем для энергий атомизации ( с учетом нулевых колебаний, трансляционной энергии и экстраполяции энтальпии образования к О К) методологически правильнее, чем такого же рода построения для энтальпий. [19]
Многочисленные экспериментальные данные свидетельствуют о том, что большинство изученных органических молекул обладают дискретными спектрами уровней энергии в основном в низших возбужденных электронных состояниях. Этот вывод получен благодаря эффекту Шпольского. [20]
Отсутствие ионных связей является важнейшим фактором, обусловливающим малую полярность большинства органических молекул в целом. [21]
Отсутствие ионных связей является важнейшим фактором, обусловливающим малую полярность большинства органических молекул в целом. Внешне это проявляется в сравнительно низких температурах плавления и кипения образованных ими веществ. Тогда как, например, NaCl плавится при 800 и кипит при 1465 С, почти все органические со едйнения плавятся и кипят ниже 300 С, а при нагревании до более высоких температур разлагаются. [22]
Отсутствие ионных связей является важнейшим фактором, обусловливающим малую полярность большинства органических молекул в целом. Внешне это проявляется в сравнительно низких температурах плавления и кипения образованных ими веществ. Тогда как, например, NaCl плавится при 800 С и кипит при 1465 С, почти все органические соединения плавятся и кипят ниже 300 С, а при нагревании до более высоких температур разлагаются. [23]
Малая полярность отдельных связей является важнейшим фактором, обусловливающим малую полярность большинства органических молекул в целом. Внешне это проявляется в сравнительно низких температурах плавления и кипения образованных ими вешеств. Тогда как, например, NaCl плавится при 800 С и кипит при 1454 С, почти все органические соединения плавятся и кипят ниже 300 С, а при нагревании до более высоких температур разлагаются. [24]
Основные полосы инфракрасного поглощения для целлюлозы расположены, так же как и для большинства органических молекул, в области 3 - 15 мкм ( 3350 - 667 см 1): В спектре целлюлозы удается разрешить около 30 полос поглощения, обладающих разной интенсивностью. Интенсивность поглощения зависит от изменения дипольного момента в процессе данного колебания. Если молекула состоит из п атомов, то число ее нормальных колебаний составляет Зп - 6; для высокомолекулярных соединений эта величина очень велика. Колебания активны только в том случае, если соответствующие атомы во всех элементарных ячейках смещаются в фазе. Это справедливо только для бесконечной полимерной цепи в кристаллической решетке. Отклонения от идеальной модели приводят к уширению полос спектра и сдвигу частот. Путем рассмотрения одной элементарной ячейки можно предсказать частоты поглощения, а для целлюлозы, основная ячейка которой содержит два остатка целлобиозы ( я 84), можно ожидать 246 нормальных колебаний. Однако взаимодействие между отдельными элементарными звеньями в макромолекуле, по-видимому, во многих случаях ничтожно и число нормальных колебаний должно быть близко к 57 - числу нормальных колебаний для одного элементарного звена. [25]
Радикалы Н взаимодействуют с растворенными веществами ( окислителями) но, вероятно, менее активны, чем радикалы ОН при взаимодействии с большинством органических молекул. [26]
Инфракрасные ( ИК) спектрометры измеряют поглощение энергии при-возбуждении молекулярных колебаний, включая валентные, деформационные и крутильные колебания различных частей молекулы, В ИК-спектрах большинства органических молекул наблюдается большое число полос и обычно невозможно отнести все полосы к конкретным молекулярным колебаниям. Однако почти для всех органических функциональных групп имеется одна или более областей характеристического поглощения. Если предполагается, что определенная функциональная группа присутствует в промежуточно образующейся частице, то при изучении изменений спектра в характеристической области, отвечающей поглощению этой функциональной группы, можно обнаружить йнтермедиат. [27]
Хотя инфракрасным излучением называют излучение с длинами волн от 0 5 до 1000 мкм, рабочий диапазон обычных лабораторных ИК-спектрометров составляет от 1 до 25 мкм; именно в этом диапазоне большинство органических молекул поглощает колебательную энергию. Для изучения спектров в других диапазонах необходимо специальное оборудование. [28]
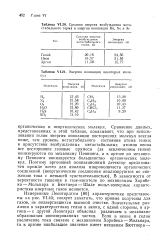 |
Средняя энергия возбуждения мета-стабильного терма и энергия ионизации Не, Ne и Аг.| Энергия ионизации некоторых молекул. [29] |
Сравнение данных, представленных в этой таблице, показывает, что при использовании гел ия энергия ионизации посторонних молекул всегда ниже, чем уровень метастабильного состояния атома гелия; в присутствии возбужденных метастабильных атомов неона все посторонние газовые примеси ( за исключением гелия) ионизируются по механизму Пеннинга, а в аргоне по механизму Пеннинга ионизируется большинство органических молекул. В зависимости от вероятности гашения в газе-носителе по механизмам Хорнбе-ка - Мольнара и Бюттнера - Шаде вольт-амперные характеристики инертных газов меняются. [30]
Страницы: 1 2 3 4