Реакция - электрофильное ароматическое замещение
Cтраница 2
Нитрование - классический и наиболее изученный пример реакций электрофильного ароматического замещения, на котором впервые устанавливались многие основные закономерности реакций этого типа. Здесь вполне надежно установлено строение и пути образования основной электрофильной частицы, ведущей эту реакцию. [16]
Роль стадии отщепления протона от а-комплекса в реакциях электрофильного ароматического замещения может быть выявлена при изучении первичного кинетического изотопного эффекта ( КИЭ) водорода. Как указывалось в разделе 13.1, для многих реакций электрофильного замещения изотопный эффект отсутствует. [17]
Роль стадии отщепления протона от комплекса в реакциях электрофильного ароматического замещения может быть выявлена при изучении первичного кинетического изотопного эффекта ( КИЭ) водорода. Как указывалось в разделе 13.1, для многих реакций электрофильного замещения изотопный эффект отсутствует. [18]
Прямых экспериментальных подтверждений участия стадии одноэлектронного переноса в реакции электрофильного ароматического замещения пока не найдено. [19]
Первый механизм не реализуется, поскольку в большинстве реакций электрофильного ароматического замещения кинетический изотопный эффект водорода не наблюдался. Например, ( нитрование С6Н6, C6D6 и С6Т6 смесью азотной и серной кислот протекает с одинаковой скоростью. Скорости нитрования CSH5NO2 и C6D5NO2 практически не отличаются, то же относится и к паре С6Н5Вг / СбТ5Вг - Отсутствие кинетического изб - ToiiHoro эффекта означает, что протон отщепляется в быстрой стадии ступенчатого процесса. Следовательно, по крайней мере для реакции нитрования синхронный механизм неприемлем, и, значит, надо принять второй механизм, в котором медленной стадией является образование аренониевого иона, а отщепление Протона происходит быстро. [20]
Первый механизм не реализуется, поскольку в большинстве реакций электрофильного ароматического замещения кинетический изотопный эффект водорода не наблюдался. Например, нитрование СбНб, C Df, и СбТб смесью азотной и серной кислот протекает с одинаковой скоростью. Скорости нитрования CeHjNC и CeDeNC практически не отличаются, тоже относится и к паре CeHsBr / CeDsBr. Отсутствие кинетического изотопного эффекта означает, что протон отщепляется в быстрой стадии ступенчатого процесса. Следовательно, по крайней мере, для реакций нитрования синхронный механизм неприемлем, и, значит, надо принять второй механизм, в котором медленной стадией является образование аренониевого иона, а отщепление протона происходит быстро. [21]
Ион-радикальную пару рассматривают как подходящую модель переходного состояния реакций электрофильного ароматического замещения. [22]
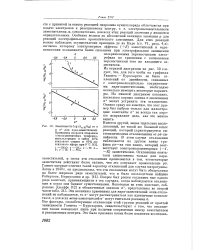 |
Зависимость log ( & п. [23] |
Особенно велики по абсолютной величине значения р для реакций электрофильного ароматического замещения. [24]
Дополнительные подтверждения того, что переходное состояние в реакциях электрофильного ароматического замещения близко по строению к а-комплексу, можно получить, изучая реакционную способность полициклических ароматических углеводородов. В этом случае различия в энергиях исходной молекулы и образующегося о-комплекса ( АЯделок) могут быть рассчитаны рядом квантовомеханических методов ( см. гл. [25]
Иенсен и Браун [115] обсудили структуру переходного состояния для реакций электрофильного ароматического замещения в связи с влиянием природы электрофильного реагента на селективность. При этом рассматривалась не только конкуренция различных реакционных центров одной молекулы, но и обсуждавшаяся выше конкуренция разных субстратов. С точки зрения этих авторов, сильный электрофил не будет ни различать в заметной степени мета - и пара-положения в атакуемом толуоле, ни атаковать толуол значительно быстрее, чем бензол. В этом случае для переходного состояния требуется относительно высокая степень связывания. Недавние опыты Ола и сотрудников наводят на мысль, что для объяснения распределения изомеров в продуктах замещения толуола, полученных в процессах, где переходное состояние напоминает зт-комплекс, может оказаться необходимой некоторая модификация этой интерпретации. [26]
Этому способствует то, что в отличие от большинства реакций электрофильного ароматического замещения, где промежуточный а-комплекс положительно заряжен, в данном случае образуется незаряженный интермедиа. Как и следовало ожидать, образование конечного продукта в этой реакции сопровождается значительным первичным кинетическим изотопным эффектом во дорода ( & H / & D 4.2), так как на скоростьопределяющей стадии происходит отрыв протона. [27]
Бифенил значительно активнее по сравнению с бензолом участвует в реакциях электрофильного ароматического замещения. [28]
В отличие от гетероциклов пиридинового типа пятичленные гетероциклы вступают в реакции электрофильного ароматического замещения только в некоординированном виде, так как связывание неподеленной пары электронов гетероатома кислотой приводит к нарушению ароматичности ( см. гл. Фуран ( 56а) особенно чувствителен к присутствию следов кислот. [29]
В отличие от них, соли тропилия не способны к реакциям электрофильного ароматического замещения. [30]
Страницы: 1 2 3 4